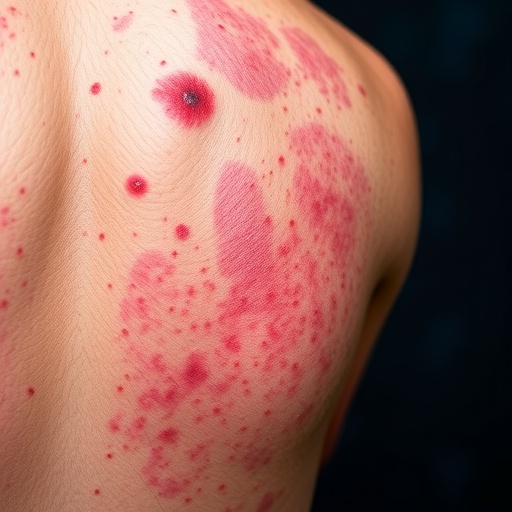
Sedefte Kişiselleştirilmiş Tedavi Dönemi: Genetik İpuçları Tanı ve İlaç Seçimini Yeniden Şekillendiriyor
Psöriazis, yalnızca deride görülen bir döküntü hastalığı olmaktan çok daha fazlası olarak kabul ediliyor. Bağışıklık sisteminin aşırı ve yanlış yönlendirilmiş yanıtıyla ilişkili bu kronik otoimmün tablo, dünya genelinde yaklaşık 125 milyon kişiyi etkiliyor ve her hastada aynı seyri göstermiyor. Kimi hastalarda sınırlı plaklarla seyreden hafif bir görünüm ortaya çıkarken, kimilerinde yaygın iltihap, eklem tutulumu ve uzun süreli alevlenmeler klinik yönetimi zorlaştırıyor. Tam da bu nedenle, hastalığın genetik ve immünolojik temellerini daha iyi anlamaya yönelik yeni bulgular, psöriaziste kişiselleştirilmiş tanı ve tedavi yaklaşımını giderek daha gerçekçi bir hedef haline getiriyor.
Genes & Immun dergisinde yayımlanan kapsamlı bir derleme, psöriazisin yalnızca tek bir mekanizmayla açıklanamayacağını; genetik yatkınlık, bağışıklık sinyalleşmesi ve çevresel etkenlerin birlikte hastalığın ortaya çıkışını ve tedavi yanıtını belirlediğini vurguluyor. Bu çerçevede en çok dikkat çeken bulgulardan biri, majör histokompatibilite kompleksi içinde yer alan HLA-C*06:02 varyantının psöriazis duyarlılığıyla güçlü ve tekrarlayan bir ilişki göstermesi oldu. Farklı popülasyonlarda benzer sonuçların elde edilmesi, bu belirtecin hastalığın genetik mimarisinde merkezi bir rol oynayabileceğine işaret ediyor.
Ancak psöriazisin genetik haritası HLA-C*06:02 ile sınırlı değil. Derlemede, IL12B ve TNIP1 gibi genlerde görülen polimorfizmlerin de hastalık biyolojisini anlamada önemli ipuçları sunduğu belirtiliyor. IL12B, interlökin-12 ve interlökin-23’ün paylaştığı bir alt birimi kodluyor; bu iki sitokin, T yardımcı hücrelerinin farklılaşmasında ve iltihap yanıtının sürdürülmesinde belirleyici kabul ediliyor. TNIP1 ise NF-κB sinyal yolunu düzenliyor. NF-κB, bağışıklık yanıtının temel kontrol merkezlerinden biri olarak biliniyor ve bu yolaktaki bozulmaların kronik inflamasyonla bağlantılı olabileceği uzun süredir araştırılıyor.
Bu genetik bulgular, psöriaziste bağışıklık sisteminin nasıl yeniden programlandığına ilişkin daha geniş bir çerçeveyle birleşiyor. Özellikle IL-23/IL-17 ekseni, hastalığın en kritik sitokin ağlarından biri olarak öne çıkıyor. Bu yolak, keratinositlerin olağandışı biçimde çoğalmasını ve inflamatuvar bağışıklık hücrelerinin lezyonlara göç etmesini destekleyen süreçlerin merkezinde yer alıyor. Artan IL-17 düzeylerinin kronik cilt inflamasyonunu beslediği, bunun da psöriyatik plakların kalıcılığında önemli rol oynadığı kabul ediliyor.
İmmünogenetik yaklaşımın klinik açıdan değeri, yalnızca hastalığın nedenini açıklamaya çalışmasından gelmiyor. Aynı zamanda hangi hastada hangi tedavinin daha etkili olabileceğini öngörme potansiyeli taşıyor. Psöriazis için kullanılan biyolojik ajanların ve hedefe yönelik tedavilerin sayısı son yıllarda artsa da, yanıt herkes için aynı değil. Bu nedenle genetik belirteçlerin, inflamatuvar yolakların ve klinik fenotipin birlikte değerlendirilmesi, “tek tip tedavi” yerine daha isabetli bir tedavi seçimi yapılmasının önünü açabilir.
Örneğin, belirli genetik profillerin bazı hastalarda belirli sitokin hedeflerini daha belirgin hale getirebileceği düşünülüyor. Bu da teorik olarak, hastanın ilk tedavide daha olası yanıt vereceği ajanların seçilmesine yardım edebilir. Benzer şekilde, hastalığın şiddeti, başlangıç yaşı, eşlik eden eklem tutulumu ve çevresel tetikleyicilerle birleşen genetik risk, daha ayrıntılı bir risk sınıflandırmasına katkı sunabilir. Yine de uzmanlar, bu alanın hızla ilerlemesine karşın klinik uygulamada genetik testlerin rutin karar verme sürecine tam olarak yerleşmediğini hatırlatıyor. Bunun temel nedeni, farklı topluluklarda doğrulama ihtiyacı, belirteçlerin öngörü gücü ve maliyet-etkinlik gibi soruların hâlâ açık olması.
Derlemenin işaret ettiği bir diğer önemli nokta, psöriazisin tek başına bağışıklık sistemi hastalığı olarak değil, çevresel etmenlerle şekillenen karmaşık bir biyolojik ağ olarak ele alınması gerektiği. Enfeksiyonlar, stres, sigara kullanımı ve bazı ilaçlar gibi tetikleyicilerin, genetik yatkınlığı olan bireylerde hastalığı görünür hale getirebildiği uzun süredir biliniyor. Bu da kişiselleştirilmiş yaklaşımın yalnızca laboratuvar testlerine değil, hastanın yaşam öyküsüne ve klinik bağlamına da dayanması gerektiğini gösteriyor.
Bilim insanlarının ilgisi şimdi, tekil biyobelirteçlerden çok çoklu veri katmanlarını bir araya getiren modellerde yoğunlaşıyor. Genetik varyantlar, sitokin profilleri, doku düzeyindeki inflamasyon ve tedavi öyküsü birlikte analiz edildiğinde, psöriazisin alt tiplerini ayırmak daha mümkün hale gelebilir. Böyle bir ayrım, hem erken tanı doğruluğunu artırabilir hem de gereksiz ilaç denemelerini azaltarak hastaların tedaviye daha hızlı ulaşmasına katkı sağlayabilir. Ancak bu yaklaşımın gerçek klinik faydaya dönüşebilmesi için daha geniş, iyi tasarlanmış ve farklı popülasyonları kapsayan çalışmalara ihtiyaç var.
Yine de mevcut veriler, psöriazis tedavisinde yeni bir dönemin kapısını aralıyor. HLA-C*06:02, IL12B, TNIP1 ve IL-23/IL-17 ekseni çevresinde şekillenen bulgular, hastalığın biyolojik imzasını çözmeye yönelik önemli adımlar olarak değerlendiriliyor. Bu bilgi birikimi, dermatologların gelecekte yalnızca belirtileri baskılayan değil, hastalığın altında yatan bağışıklık düzenini de dikkate alan daha hedefli kararlar vermesine yardımcı olabilir. Psöriaziste “kişiselleştirilmiş tıp” kavramı henüz tam olgunlaşmış değil; ancak immunogenetik araştırmalar, bu hedefe şimdiye kadarki en somut yaklaşımlardan birini sunuyor.

 MIT ve MGH’den mRNA Aşılarını T Hücrelerinde Güçlendiren Yeni Kanser Aşısı Yaklaşımı
MIT ve MGH’den mRNA Aşılarını T Hücrelerinde Güçlendiren Yeni Kanser Aşısı Yaklaşımı
 Perimenopoz Dönemi, Kalp Sağlığı İçin Beklenenden Daha Erken Bir Uyarı Penceresi Olabilir
Perimenopoz Dönemi, Kalp Sağlığı İçin Beklenenden Daha Erken Bir Uyarı Penceresi Olabilir
 Demans Bakımında Yeni Yol Haritası: Evde Destek İçin Sağlık ve Sosyal Hizmetler Aynı Masada
Demans Bakımında Yeni Yol Haritası: Evde Destek İçin Sağlık ve Sosyal Hizmetler Aynı Masada






