
MIT ve MGH’den mRNA Aşılarını T Hücrelerinde Güçlendiren Yeni Kanser Aşısı Yaklaşımı
Massachusetts Teknoloji Enstitüsü’nden (MIT) araştırmacılar, mRNA aşılarının bağışıklık sisteminde oluşturduğu T hücresi yanıtını belirgin biçimde artırabilecek yeni bir strateji geliştirdi. Çalışma, yalnızca antikor üretimini değil, özellikle hedef hücreleri tanıyıp yok edebilen T hücrelerinin daha güçlü ve kalıcı biçimde devreye sokulmasını amaçlıyor. Bu yaklaşım, kanser immünoterapisi açısından dikkat çekici bir potansiyel taşırken, enfeksiyonlara karşı geliştirilen aşıların etkinliğini artırmaya yönelik daha geniş bir kapı da aralayabilir.
Aşı bilimi uzun süredir bağışıklık sisteminin iki ana kolunu aynı anda harekete geçirmeye çalışıyor: antikorlar ve T hücreleri. Antikorlar, patojenleri ya da hedef antijenleri nötralize etmede kritik rol oynarken, T hücreleri özellikle tümör hücreleri gibi vücudun içindeki tehditleri tanıyıp ortadan kaldırabilen daha doğrudan bir savunma mekanizması sunuyor. Ancak T hücresi yanıtını yeterince güçlü ve sürdürülebilir biçimde uyarmak, özellikle kanser aşılarında halen zorlayıcı bir hedef olmaya devam ediyor. MIT ekibinin çalışması, tam da bu sınıra odaklanarak bağışıklık yanıtını yönlendiren hücresel programları yeniden düzenleyen bir adjuvan yaklaşımı öneriyor.
Geliştirilen yöntem, klasik anlamda bağışıklık sistemini genel olarak uyaran adjuvanlardan farklılaşıyor. Araştırmacılar, belirli bağışıklık düzenleyici genleri kodlayan mRNA moleküllerini kullanarak dendritik hücreleri yeniden programladı. Dendritik hücreler, bağışıklık sisteminde antijen sunan ve T hücrelerini “eğiten” temel hücre gruplarından biri olarak biliniyor. Bu hücreler yeterince etkin çalıştığında, T hücrelerinin hedefi tanıma ve saldırı kapasitesi de artıyor. Yeni yaklaşımın temel fikri, dendritik hücreleri yalnızca uyarılmış bir duruma getirmek değil, onları T hücresi aktivasyonuna daha elverişli, daha yüksek performanslı bir duruma taşımak.
Çalışmada öne çıkan iki gen IRF8 ve NIK oldu. IRF8, bağışıklık hücrelerinin kimliğini ve işlevini şekillendirmede önemli rol oynayan bir transkripsiyon faktörü olarak biliniyor. NIK ise bağışıklık sinyal yollarının düzenlenmesinde görev alan bir protein. Araştırma ekibi, bu iki bileşeni kodlayan mRNA’ların dendritik hücrelerin davranışını değiştirerek daha güçlü T hücresi aktivasyonu sağladığını gösterdi. Bulgular, adjuvanın bağışıklık hücresini yalnızca “aktif” hale getirmekle kalmayıp, antijen sunumu ve sinyal iletimini T hücresi yanıtını büyütecek şekilde yeniden ayarladığını düşündürüyor.
Bu tür bir strateji, mRNA teknolojisinin son yıllardaki yükselişiyle de yakından bağlantılı. mRNA aşıları, hücrelere geçici olarak belirli proteinleri üretmeleri için genetik talimat verir; böylece bağışıklık sistemi hedefe karşı eğitim alır. Ancak mRNA platformunun başarısı sadece hangi antijenin kodlandığına değil, bağışıklık mikroçevresinin nasıl şekillendirildiğine de bağlıdır. MIT’nin yaklaşımı, antijen içeriğine ek olarak immün yanıtın kalitesini belirleyen hücresel programı güçlendirmeye odaklanıyor. Bu durum, aynı platformun hem kanser aşılarında hem de enfeksiyon hastalıklarına karşı geliştirilecek aşı tasarımlarında neden önemli görüldüğünü açıklıyor.
Özellikle kanserde T hücresi yanıtının gücü ve sürekliliği hayati önem taşıyor. Tümörler, bağışıklık sisteminden kaçmak için çeşitli mekanizmalar geliştirebildiğinden, sıradan bir bağışıklık aktivasyonu çoğu zaman yeterli olmuyor. Bu nedenle araştırmacılar, yalnızca bağışıklığı uyarmak yerine onu daha doğru yönlendiren ve dendritik hücrelerin işlevini artıran çözümlere yöneliyor. MIT çalışmasının işaret ettiği yeni adjuvan yaklaşımı da bu bağlamda, daha etkili antitümör yanıtlar oluşturabilecek bir araç olarak değerlendiriliyor. Araştırma, hatta mevcut kontrol noktası baskılayıcı tedavilerle birlikte kullanıldığında, daha kapsamlı bir bağışıklık etkisi oluşturulabileceğini düşündürüyor; ancak bu tür kombinasyonların klinik yararı henüz doğrulanmış değil.
Çalışmanın bir diğer önemli yönü, bağışıklık düzenlemesinin daha hassas bir şekilde yapılabilmesi. Geleneksel adjuvanlar çoğu zaman geniş ve bazen öngörülemez bir inflamatuvar etki oluştururken, gen temelli yaklaşım belirli hücresel yolakları hedefleme avantajı sunuyor. Bu, teorik olarak hem etkinliği artırabilir hem de istenmeyen bağışıklık yanıtlarını sınırlamaya yardımcı olabilir. Yine de uzmanlar açısından bu tür bir stratejinin klinik uygulamaya taşınması için güvenlik, doz, hedef dokulara ulaşım ve uzun dönem etkiler gibi başlıkların ayrıntılı biçimde incelenmesi gerekiyor.
MIT ekibinin elde ettiği sonuçlar, kanser aşıları için daha güçlü bir bağışıklık mimarisi kurma arayışında önemli bir adım olarak görülüyor. Dendritik hücreleri yeniden programlayan mRNA temelli adjuvanlar, mRNA platformunun yalnızca antijen taşıyan bir sistem olmadığını; bağışıklık yanıtının niteliğini aktif biçimde şekillendirebilen bir araç haline gelebileceğini gösteriyor. Bu tür çalışmalar, kişiselleştirilmiş kanser aşılarından bulaşıcı hastalık aşılarına kadar uzanan geniş bir yelpazede geleceğin tasarımlarını etkileyebilir. Ancak araştırma erken aşamadaki bulgulara dayanıyor ve insanlarda uygulanabilirliğin doğrulanması için ek deneysel ve klinik değerlendirmelere ihtiyaç var.
Yine de sonuçların işaret ettiği yön net: Eğer dendritik hücreler daha verimli biçimde programlanabilirse, mRNA aşıları yalnızca bağışıklık sistemini uyaran değil, onu daha isabetli ve güçlü çalıştıran platformlara dönüşebilir. Bu da kanser immünoterapisi alanında uzun süredir aranan daha etkili T hücresi aktivasyonuna bir adım daha yaklaşmak anlamına geliyor.

 Perimenopoz Dönemi, Kalp Sağlığı İçin Beklenenden Daha Erken Bir Uyarı Penceresi Olabilir
Perimenopoz Dönemi, Kalp Sağlığı İçin Beklenenden Daha Erken Bir Uyarı Penceresi Olabilir
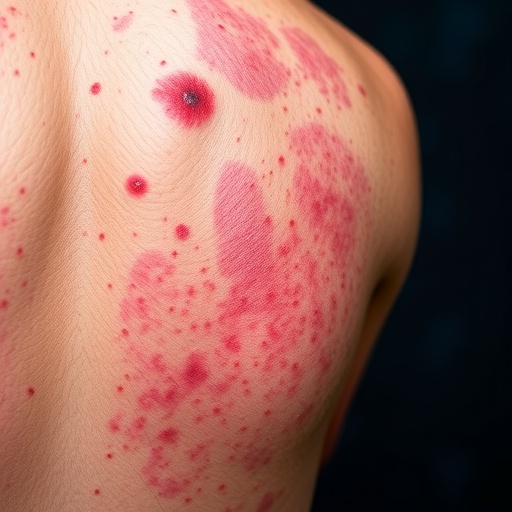 Sedefte Kişiselleştirilmiş Tedavi Dönemi: Genetik İpuçları Tanı ve İlaç Seçimini Yeniden Şekillendiriyor
Sedefte Kişiselleştirilmiş Tedavi Dönemi: Genetik İpuçları Tanı ve İlaç Seçimini Yeniden Şekillendiriyor
 Demans Bakımında Yeni Yol Haritası: Evde Destek İçin Sağlık ve Sosyal Hizmetler Aynı Masada
Demans Bakımında Yeni Yol Haritası: Evde Destek İçin Sağlık ve Sosyal Hizmetler Aynı Masada






