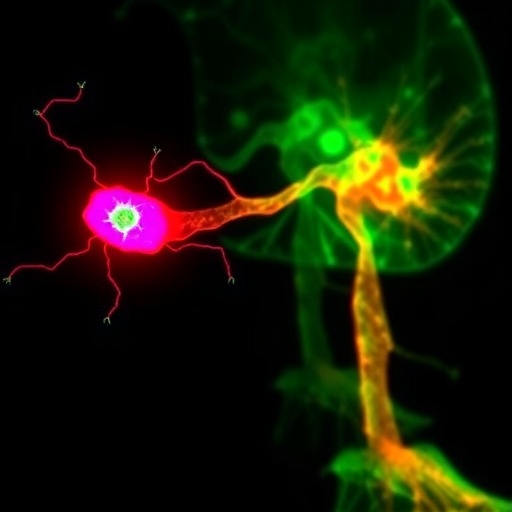
Keloidlerde Sinirlerden Gelen Sinyaller Kemikleşme Eğilimini Tetikliyor
Bilim insanları, keloidlerin yalnızca aşırı kolajen birikimiyle değil, aynı zamanda beklenmedik bir “kemikleşme” eğilimiyle de şekillendiğini ortaya koyan dikkat çekici bir çalışma yayımladı. Nature Communications’ta 2026’da yayımlanan araştırma, katekolaminerjik nöronların keloid fibroblastlarını osteojenik, yani kemik oluşturmaya yatkın bir programa doğru yönlendirebildiğini gösteriyor. Bu bulgu, uzun zamandır yalnızca yara iyileşmesinin kontrolden çıkmış bir biçimi olarak değerlendirilen keloid patolojisine sinir sistemiyle bağlantılı yeni bir boyut ekliyor.
Keloidler, hasar görmüş derinin sınırlarını aşarak büyüyen, sert ve kabarık skar dokularıyla biliniyor. Klinik açıdan sorun, bu lezyonların yalnızca kozmetik bir iz bırakmasından ibaret değil; kaşıntı, ağrı, gerginlik ve hareket kısıtlılığı gibi yakınmalara da yol açabiliyor. Araştırmacılar, şimdiye kadar çoğunlukla fibroblastların aşırı çoğalması ve yoğun kolajen üretimi üzerinden açıklanan bu tabloya, hücreler arası yeni bir etkileşim ekliyor: sinir hücrelerinden gelen katekolamin sinyalleri, keloid fibroblastlarını kemik-benzeri doku üretimine daha yatkın hale getiriyor.
Lou, Liang, Sun ve çalışma arkadaşlarının yürüttüğü araştırma, keloid dokusunda yalnızca fibrotik hücre davranışını değil, doku içindeki sinirsel bileşeni de inceleyerek dikkat çekiyor. Ekip, tek hücre RNA dizileme gibi ileri teknolojiler ve nörogörüntüleme yöntemleri kullanarak skar mikroçevresini ayrıntılı biçimde haritaladı. Bulgular, keloid matriksi içinde katekolaminerjik nöronların zenginleştiğini ve bu hücrelerin fibroblastlara yakın konumlandığını gösterdi. Bu komşuluk, yalnızca anatomik bir ayrıntı gibi görünmüyor; araştırmaya göre doğrudan işlevsel bir etkileşim anlamına geliyor.
Katekolaminerjik nöronlar dopamin, norepinefrin ve epinefrin gibi katekolaminleri sentezleyen sinir hücreleri olarak bilinir. Bu moleküller genellikle sinir iletimi ve stres yanıtı bağlamında düşünülür. Ancak yeni çalışma, bu klasik nörobiyolojik rolün ötesinde, söz konusu sinyallerin fibroblastların kaderini de değiştirebildiğine işaret ediyor. Araştırma ekibi, katekolaminlerin parakrin bir mekanizmayla, yani yakın çevredeki hücreleri etkileyerek, keloid fibroblastlarını osteojenik yollara ittiğini ortaya koydu. Başka bir ifadeyle, skar dokusu içindeki sinirsel sinyaller fibroblastların sadece skar üreten hücreler olarak kalmasını değil, kemik yapımına benzer özellikler kazanmasını da destekleyebiliyor.
Bu dönüşümün neden önemli olduğu, keloidlerin yapısal sertliğinde saklı. Fibroblastların osteojenik farklılaşmaya kayması, dokuda kemik-benzeri bir sertlik ve anormal matriks organizasyonu oluşumunu güçlendirebilir. Araştırmacılar, bu durumun keloidlerin alışılmışın dışında katı ve dirençli yapısına katkı sağlayabileceğini belirtiyor. Çalışma, fibroblastların içinde zaten var olan bir osteojenik potansiyelin bulunduğunu, ancak katekolaminerjik sinyallerle bu potansiyelin belirgin biçimde artırıldığını düşündürüyor. Bu açıdan bakıldığında, keloid yalnızca onarımın aşırıya kaçmış hali değil, aynı zamanda sinir ve bağ dokusu arasındaki etkileşimin yeniden programlandığı bir mikroçevre olabilir.
Bilimsel açıdan en dikkat çekici noktalardan biri, bu bulguların deri biyolojisinde “nörokutanöz eksen” olarak adlandırılabilecek yeni bir çerçeve önermesi. Deri, bağışıklık sistemi, damar yapıları ve fibroblastlar arasındaki ilişki uzun süredir araştırılıyordu; ancak sinir hücrelerinin skar biyolojisindeki yönlendirici rolü daha az anlaşılmıştı. Bu çalışma, sinir sisteminin yalnızca ağrı veya duyusal uyarı iletmediğini, aynı zamanda yara iyileşmesi sürecinde hangi hücrelerin hangi yönde farklılaşacağını etkileyebildiğini düşündürüyor. Böylece keloid oluşumu, yalnızca lokal bağ dokusu anormalliği olarak değil, sinirsel sinyallerle şekillenen çok hücreli bir süreç olarak yeniden yorumlanıyor.
Elbette bu bulgular, klinik uygulamaya doğrudan çevrilebilecek bir tedaviden çok, keloid biyolojisini anlamaya yönelik temel bir adım niteliğinde. Araştırma, insanlarda keloid gelişimini tek başına açıklayan nihai bir mekanizma sunduğunu iddia etmiyor; ancak fibroblast davranışını düzenleyen sinyal ağlarına yeni bir kapı açıyor. Eğer ileride bu eksen daha ayrıntılı biçimde doğrulanırsa, katekolamin sinyallemesini veya sinir-fibroblast etkileşimini hedefleyen stratejiler, keloidlerin sertleşmesini ya da ilerlemesini sınırlamaya dönük yeni yaklaşımların temelini oluşturabilir. Şimdilik ise bu, özellikle dirençli skar dokularında sinirsel çevrenin sanılandan çok daha etkili olabileceğini gösteren güçlü bir kanıt olarak öne çıkıyor.
Çalışmanın bir diğer önemi, keloidleri yalnızca estetik bir sorun olarak gören yaklaşımı aşması. Keloid patolojisinin hücresel ve moleküler temelleri daha iyi anlaşıldıkça, bu lezyonların neden bazı bireylerde yoğunlaştığı, neden kimi dokularda daha sert ve kalıcı hale geldiği ve neden standart tedavilere sınırlı yanıt verdiği gibi sorular daha net yanıtlar bulabilir. Yeni veriler, fibroblastların çevresel uyarılara son derece duyarlı olduğunu ve bu hücrelerin sinir kökenli sinyallerle beklenmedik biçimde farklılaşabildiğini gösteriyor.
Sonuç olarak, Lou ve meslektaşlarının çalışması keloid araştırmalarında önemli bir dönüm noktası oluşturuyor. Katekolaminerjik nöronların fibroblast osteojenezini artırdığına dair bulgular, skar dokusunun biyolojisine sinir sistemi perspektifinden bakmanın ne kadar değerli olabileceğini ortaya koyuyor. Bu da ileride, keloidlerin daha iyi anlaşılması ve hedefe yönelik tedavilere zemin hazırlanması açısından umut verici bir bilimsel yönelim olarak dikkat çekiyor.

 MIT ve MGH’den mRNA Aşılarını T Hücrelerinde Güçlendiren Yeni Kanser Aşısı Yaklaşımı
MIT ve MGH’den mRNA Aşılarını T Hücrelerinde Güçlendiren Yeni Kanser Aşısı Yaklaşımı
 Perimenopoz Dönemi, Kalp Sağlığı İçin Beklenenden Daha Erken Bir Uyarı Penceresi Olabilir
Perimenopoz Dönemi, Kalp Sağlığı İçin Beklenenden Daha Erken Bir Uyarı Penceresi Olabilir
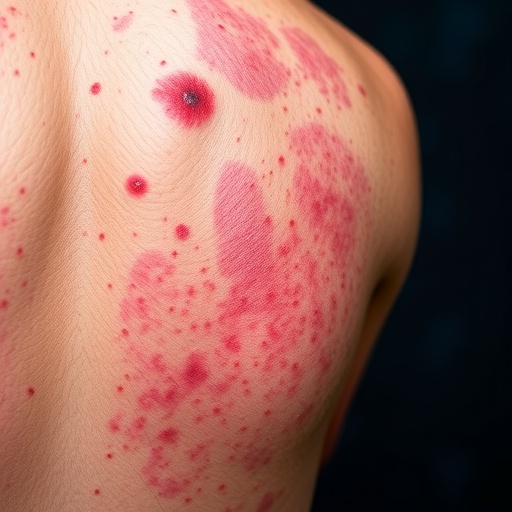 Sedefte Kişiselleştirilmiş Tedavi Dönemi: Genetik İpuçları Tanı ve İlaç Seçimini Yeniden Şekillendiriyor
Sedefte Kişiselleştirilmiş Tedavi Dönemi: Genetik İpuçları Tanı ve İlaç Seçimini Yeniden Şekillendiriyor






