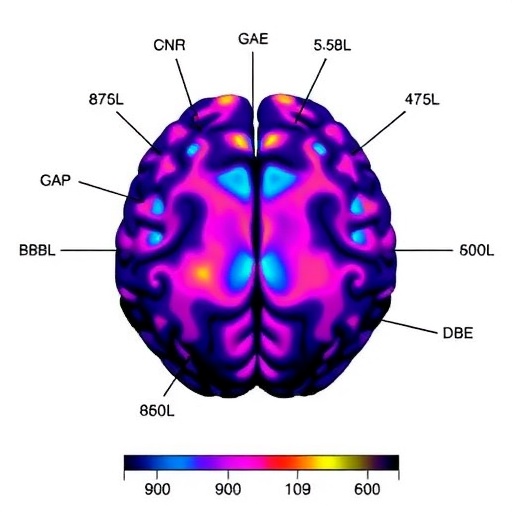
Parkinson’da Amygdala Lipitleri: GBA ile Sporadik Olgular Arasında Yeni Ayrımlar
Parkinson hastalığının yalnızca hareket bozukluğu yaratan bir dopamin kaybı tablosu olmadığı artık uzun süredir biliniyor; ancak yeni bir çalışma, hastalığın beynin daha az öne çıkan bölgelerindeki biyokimyasal izlerine dair çok daha ayrıntılı bir pencere açıyor. Muñoz, Marlet, Dreier ve meslektaşlarının kısa süre içinde npj Parkinson’s Disease dergisinde yayımlanması beklenen araştırması, amigdalanın lipid yapısını inceleyerek sporadik Parkinson hastalığı ile glukoserebrozidaz (GBA) genindeki mutasyonlarla ilişkili Parkinson hastalığı arasında hem ortak hem de farklılaşan özellikler bulunduğunu ortaya koyuyor.
Çalışmanın dikkati amigdala üzerine çevirmesi önemli, çünkü bu beyin bölgesi çoğu zaman duygulanım ve bellekle ilişkilendirilse de Parkinson patolojisinde de anlamlı değişiklikler gösteriyor. Hastalık klasik olarak substantia nigra’daki dopaminerjik nöron kaybıyla anılsa da, son yıllardaki veriler patolojinin daha geniş bir anatomik dağılım sergilediğini gösteriyor. Araştırmacılar da bu nedenle amigdalanın biyokimyasal ortamını, özellikle de hücre zarı yapısı, sinyal iletimi ve nöroinflamasyon açısından kritik rol oynayan lipit bileşenlerini mercek altına aldı.
Bu yaklaşım, hastalığın yalnızca protein birikimi ya da nöronal dejenerasyon üzerinden okunamayacağını hatırlatıyor. Lipitler, sinir hücrelerinin zar özelliklerini belirlemekle kalmaz; aynı zamanda hücreler arası iletişim, stres yanıtı ve inflamatuvar süreçlerde de aktif rol oynar. Parkinson’da bu dengenin bozulmasının, hastalığın farklı beyin bölgelerinde farklı biçimlerde ilerlemesine katkı sağlayabileceği düşünülüyor. Özellikle GBA genindeki değişiklikler, lizozomal işlev ve hücresel yıkım süreçleriyle bağlantıları nedeniyle Parkinson biyolojisinde ayrı bir önem taşıyor.
Çalışmada kullanılan yöntem de dikkat çekici. Araştırmacılar, postmortem amigdala dokularında kütle spektrometrisine dayalı, hedeflenmemiş bir lipidomik analiz uyguladı. Bu tür analizler, önceden seçilmiş birkaç lipid sınıfıyla sınırlı kalmadan, dokuda bulunan çok sayıda lipid türünü kapsamlı biçimde taramayı mümkün kılıyor. İncelenen örnekler sporadik Parkinson hastalarından, GBA ilişkili Parkinson hastalarından ve uygun kontrol gruplarından elde edildi. Böylece hem genetik açıdan tanımlı hem de idiopatik olguların lipid profilleri karşılaştırılabildi.
Bu tür karşılaştırmalar, Parkinson’un tek bir biyolojik yolaktan ibaret olmadığını göstermesi bakımından değerli. Sporadik olgular ile GBA mutasyonu taşıyan hastalar, klinik olarak benzer belirtiler sergilese de altta yatan hücresel süreçler aynı olmayabilir. Çalışmanın asıl gücü de burada yatıyor: amigdala dokusundaki lipid düzenlerinin benzerliklerini ve ayrışan yönlerini haritalayarak, Parkinson alt tiplerinin moleküler düzeyde nasıl ayrışabileceğine dair yeni ipuçları sunuyor.
Henüz erken aşamada olan bu araştırmanın sonuçları, doğrudan tedaviye çevrilebilir bir bulgu olarak yorumlanmamalı. Bununla birlikte, lipit metabolizmasının Parkinson patogenezindeki rolüne ilişkin mevcut bilimsel çerçeveyi güçlendirdiği açık. Özellikle GBA ile ilişkili olgularda lizozomal bozulma ve lipid işlenmesindeki aksaklıkların, beyin dokularında belirgin biyokimyasal farklılıklar yaratabileceği düşüncesi, bu çalışmayla daha somut bir zemin kazanıyor. Aynı zamanda amigdalanın incelenmesi, motor olmayan belirtilerin ve yaygın nöropatolojik etkilerin anlaşılması açısından da önem taşıyor.
Parkinson araştırmalarında bugüne kadar sıklıkla substantia nigra ve striatal sistem üzerine yoğunlaşılmış olsa da, bu çalışma hastalığın duygusal ve bilişsel işlevlerle ilişkili bölgelerinde de ayrıntılı moleküler değişiklikler olabileceğini hatırlatıyor. Amigdala lipitlerindeki değişimler, yalnızca hücresel zar bütünlüğünü değil, aynı zamanda nöronal iletişimi ve iltihabi yanıtları da etkileyebileceğinden, hastalığın karmaşık klinik görünümünü anlamada önemli olabilir. Bu da özellikle hastalığın farklı genetik alt gruplarında patolojinin neden değişken seyredebildiğine ilişkin sorulara yanıt arayan çalışmalar için yeni bir başlangıç noktası oluşturuyor.
Yine de araştırmanın niteliği göz önünde bulundurularak temkinli değerlendirme yapılmalı. Postmortem doku analizi, hastalığın yaşam boyu dinamiklerini doğrudan göstermez ve gözlenen lipid değişiklikleri nedensel mi yoksa hastalığın sonucu mu, bu aşamada kesin olarak söylenemez. Buna karşın, güçlü analitik yöntemlerle elde edilen bu tür veriler, Parkinson’da biyobelirteç arayışları ve hedefli mekanizma çalışmaları için önemli bir temel oluşturur. Özellikle genetik ve sporadik hastalık ayrımının aynı beyin bölgesinde lipid düzeyinde izlenmesi, daha kişiselleştirilmiş araştırma stratejilerine kapı aralayabilir.
Muñoz ve arkadaşlarının çalışması, Parkinson hastalığına dair anlayışın giderek daha fazla katman kazandığını gösteriyor. Amigdala gibi geleneksel motor devrelerin dışında kalan bölgelerde yapılan ayrıntılı lipidomik incelemeler, hem hastalığın biyolojik çeşitliliğini hem de genetik etkenlerin beyin kimyası üzerindeki etkisini daha net ortaya koyabilir. Önümüzdeki dönemde yayımlanacak tam makale, bu ortak ve farklı lipid imzalarının hangi moleküler yollarla ilişkili olduğunu daha ayrıntılı biçimde gösterecek ve Parkinson’un alt tiplerine dair tartışmalara yeni bir boyut ekleyecek gibi görünüyor.

 Kore Üniversitesi Tıbbı, En Büyük BL3 ve ABL3 Laboratuvarlarını Hizmete Açtı
Kore Üniversitesi Tıbbı, En Büyük BL3 ve ABL3 Laboratuvarlarını Hizmete Açtı
 Mitokondride Enerji Kontrolüne MICU İmzası: Kalsiyum Sinyali Hakkında Ezber Bozan Bulgular
Mitokondride Enerji Kontrolüne MICU İmzası: Kalsiyum Sinyali Hakkında Ezber Bozan Bulgular
 Prostat Kanserinde Docetaxel Direncini Açıklayan Yeni Epigenetik İz: Histon Laktillasyonu
Prostat Kanserinde Docetaxel Direncini Açıklayan Yeni Epigenetik İz: Histon Laktillasyonu






