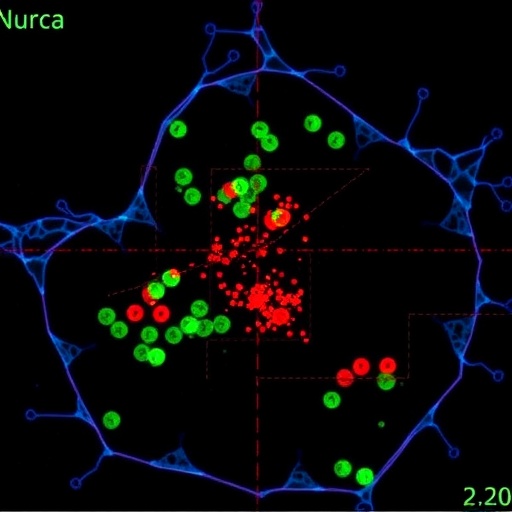
Nükleusta Sessiz Bir Kontrol Katmanı: mTORC1’e Hedefli Müdahale Gen İfadesini Aydınlatıyor
Hücrelerin büyüme, beslenme ve enerji dengesini nasıl ayarladığı uzun süredir biyolojinin merkezindeki sorulardan biri. Son dönemde Nature Chemical Biology’de yayımlanan Zhong ve çalışma arkadaşlarının araştırması, bu temel soruya yeni bir boyut ekliyor: Araştırmacılar, mTORC1 adlı ana sinyal kompleksini doğrudan nükleusta hedefleyen genetik olarak yönlendirilmiş bir inhibitör geliştirerek, bu yapının yalnızca sitoplazmadaki klasik görevleriyle sınırlı olmadığını, aynı zamanda gen transkripsiyonunu da kontrol ettiğini ortaya koydu.
mTORC1, yani mekanik hedef rapamisin kompleksi 1, hücre içinde besin kaynakları, büyüme faktörleri ve çevresel koşullardan gelen sinyalleri birleştiren önemli bir düzenleyici olarak biliniyor. Bugüne kadar bu kompleks daha çok protein sentezi, lipit metabolizması ve otofaji gibi sitoplazmik süreçlerle ilişkilendiriliyordu. Ancak kompleksin çekirdek içindeki davranışı, teknik sınırlamalar nedeniyle uzun süre net biçimde incelenemedi. Zhong ve ekibinin geliştirdiği araç tam da bu boşluğu hedefliyor: mTORC1’i genel olarak kapatmak yerine, seçici biçimde nükleer havuzunu baskılayan bir moleküler yaklaşım.
Araştırmanın dikkat çekici yönü, bu inhibitörün yalnızca bir müdahale aracı değil, aynı zamanda bir “moleküler prob” gibi çalışması. Yani bilim insanları, mTORC1’in nükleustaki varlığını pasif olarak gözlemek yerine, onu seçici olarak devre dışı bırakarak hangi genlerin ve hangi transkripsiyon programlarının etkilenmiş olduğunu doğrudan inceleyebiliyor. Bu yaklaşım, hücresel sinyal iletimiyle gen düzenlenmesi arasındaki bağlantıyı daha keskin bir şekilde ayırmayı mümkün kılıyor. Özellikle de mTORC1’in çekirdek içinde gerçekten işlevsel olup olmadığına dair uzun süredir tartışılan soruya güçlü bir deneysel çerçeve sunuyor.
Çalışmanın işaret ettiği sonuç, nükleer mTORC1’in hücre kaderini belirleyen gen ifadelerini aktif biçimde etkilediği yönünde. Bu, kompleksin yalnızca büyüme için gerekli biyokimyasal süreçleri destekleyen bir üst düzenleyici olmaktan öteye geçtiğini gösteriyor. Başka bir deyişle, mTORC1 artık yalnızca hangi proteinlerin üretileceğini dolaylı biçimde belirleyen bir “metabolik anahtar” değil, aynı zamanda belirli gen programlarını yönlendiren bir çekirdek denetleyicisi olarak da değerlendirilmeye başlıyor.
Bu bulgunun önemi, hücre biyolojisinde bölmeler arası görev paylaşımını yeniden düşünmeyi gerektirmesinde yatıyor. Bir sinyal yolunun sitoplazmada etkin olması ile çekirdekte doğrudan transkripsiyonu etkilemesi arasındaki fark, hem temel araştırmalar hem de tedavi tasarımı açısından belirleyici olabilir. Çünkü genel mTORC1 baskılanması, hücrenin birçok işlevine aynı anda müdahale eder ve istenmeyen yan etkiler doğurabilir. Buna karşılık, yalnızca nükleer mTORC1’i hedefleyen seçici bir strateji, teorik olarak daha rafine ve daha hassas müdahale yollarının kapısını aralayabilir. Yine de bu tür uygulamaların klinik kullanıma dönüşmesi için daha fazla doğrulama ve kapsamlı güvenlik değerlendirmesi gerekeceği açık.
Araştırma ayrıca, mTORC1’in metabolizma ile gen ifadesi arasındaki ilişkiyi nasıl köprülediğine dair daha incelikli bir tablo sunuyor. Hücreler enerji ve besin durumlarına göre büyüme programlarını ayarlar; bu nedenle mTORC1, anabolik süreçlerin merkezinde yer alır. Ancak yeni çalışma, bu düzenlemenin yalnızca kısa vadeli biyokimyasal değişimlerden ibaret olmadığını, çekirdek içindeki transkripsiyonel kararlarla da bağlantılı olabileceğini gösteriyor. Bu, hücrelerin çevresel koşullara verdiği yanıtın çok katmanlı olduğunu ve farklı hücresel kompartımanlarda eş zamanlı işleyen kontrol mekanizmaları barındırdığını düşündürüyor.
Bilim insanları açısından bu tür bir araç, yalnızca tek bir yolu anlamakla kalmıyor; aynı zamanda başka soruları da görünür kılıyor. Nükleer mTORC1 hangi gen kümelerini etkiliyor? Bu etki doğrudan mı gerçekleşiyor, yoksa başka çekirdek içi düzenleyiciler aracılığıyla mı? Farklı hücre tiplerinde aynı mekanizma korunuyor mu? Zhong ve ekibinin çalışması bu soruların tümünü yanıtlamıyor, ancak alanı daha yüksek çözünürlüklü deneylere taşıyacak bir yöntem sunuyor. Özellikle gen düzenleme, hücre büyümesi ve metabolik yeniden programlama üzerine çalışan araştırmacılar için bu, önemli bir teknik eşik anlamına geliyor.
Daha geniş perspektiften bakıldığında, bulgu biyomedikal araştırmaların giderek daha fazla “yerel hedefleme” yaklaşımına yöneldiğini de yansıtıyor. Bir proteini tamamen susturmak yerine, onun belirli bir hücre bölmesindeki işlevini ayırmak; hem biyolojik anlamayı derinleştiriyor hem de terapötik tasarıma daha hassas bir zemin hazırlıyor. mTORC1 örneğinde bu ayrım özellikle kritik, çünkü kompleksin normal fizyolojik görevleri ile hastalık süreçlerindeki aşırı aktivitesi arasında hassas bir denge bulunuyor. Buna karşın, bu çalışma hastalık tedavisi için doğrudan bir çözüm sunduğu iddiasında değil; daha çok, gelecekteki hedefli yaklaşımlar için sağlam bir bilimsel altyapı oluşturuyor.
Sonuç olarak Zhong ve meslektaşlarının geliştirdiği genetik olarak hedeflenmiş mTORC1 inhibitörü, mTORC1 biyolojisinde önemli bir dönüm noktasına işaret ediyor. Araç, nükleer mTORC1’in transkripsiyon üzerindeki etkisini görünür kılarak hücre büyümesi, metabolizma ve gen düzenlenmesi arasındaki ilişkiye dair yerleşik çerçeveyi genişletiyor. Çalışma, çekirdeğin yalnızca genetik bilginin saklandığı bir alan değil, aynı zamanda büyüme sinyallerinin aktif biçimde yorumlandığı bir kontrol merkezi olabileceğini güçlü biçimde ortaya koyuyor. Bu da hem temel biyoloji hem de geleceğin hassas tedavi stratejileri için yeni bir araştırma hattı açıyor.

 Akıllı Nanoplatformlar Kanser Tedavisinde Kişiselleştirilmiş Dönemi İleri Taşıyor
Akıllı Nanoplatformlar Kanser Tedavisinde Kişiselleştirilmiş Dönemi İleri Taşıyor
 Gebelikte Maruz Kalınan Kimyasal Karışımlar Plasenta Üzerinden Bebeğin Büyümesini Etkileyebilir
Gebelikte Maruz Kalınan Kimyasal Karışımlar Plasenta Üzerinden Bebeğin Büyümesini Etkileyebilir
 Normal Endoskopiye Rağmen Omurgaya Ulaşan Nadide Yemek Borusu Kanseri Vakası Tıpta Alarm Zillerini Çaldı
Normal Endoskopiye Rağmen Omurgaya Ulaşan Nadide Yemek Borusu Kanseri Vakası Tıpta Alarm Zillerini Çaldı






