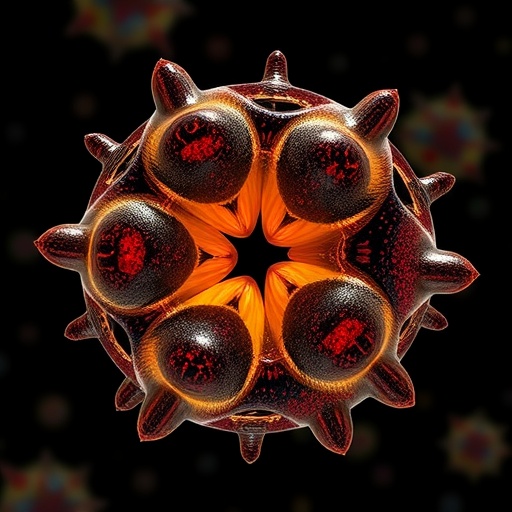
Yapay Hücrelerde Asimetrik Bölünmeye Giden Yeni Yol: Lipid-Nükleotit Damlacıkları
Sentetik biyoloji alanında çalışan araştırmacılar, canlı hücrelerin en ayırt edici özelliklerinden biri olan asimetrik bölünmeye yaklaşan dikkat çekici bir mekanizmayı ortaya çıkardı. Nature’da yayımlanan ve Meng, Jia, Qiu ile çalışma arkadaşlarının imzasını taşıyan araştırma, çok katmanlı lipid-nükleotit damlacıklarının dışarıdan karmaşık protein makinelerine ihtiyaç duymadan, kendiliğinden eşitsiz biçimde ayrılabildiğini gösteriyor. Bu bulgu, yapay hücrelerin yalnızca bölünmesini değil, aynı zamanda farklı özellikler taşıyan yavru yapılar üretmesini mümkün kılabilecek yeni bir tasarım ilkesi sunuyor.
Çalışmanın merkezinde yer alan sistemler, sıvı kristal özellikler gösteren ve biyomoleküller açısından yoğun iç yapılara sahip mikroskobik damlacıklar. Bu tür protosel benzeri düzenekler, hücrelerin içerideki maddeleri bölmelere ayırma, belirli molekülleri seçici biçimde toplama ve farklı kimyasal mikroçevreler oluşturma gibi temel davranışlarını taklit edebildikleri için uzun süredir ilgi görüyor. Ancak bu yapılarda bölünme çoğu zaman yalnızca eşit parçalanma şeklinde gerçekleşiyordu. Yani tek bir ebeveyn yapı, benzer boyutta ve benzer içerikte iki yavruya ayrılabiliyordu. Bu durum, biyolojik hücrelerde görülen daha gelişmiş çoğalma ve farklılaşma süreçlerini modellemek için yeterli değildi.
Canlı sistemlerde asimetrik bölünme son derece önemlidir; çünkü bölünen hücrelerden biri diğerinden yapısal ya da işlevsel olarak farklılaşabilir. Bu mekanizma, gelişim biyolojisinden kök hücre davranışına kadar çok geniş bir alanda belirleyici rol oynar. Sentetik biyolojideyse aynı ilke, yapay hücrelerin yalnızca kopyalanan kabuklar değil, görev dağılımı yapabilen dinamik sistemler haline gelmesi açısından kritik görülüyor. Meng ve arkadaşlarının çalışması, bu hedefe yönelik önemli bir adım olarak değerlendiriliyor; çünkü araştırmacılar, çok katmanlı lipid-nükleotit damlacıklarının belirli biyokimyasal tetikleyicilerle dengesiz biçimde bölünebildiğini gösterdi.
Elde edilen sonuca göre, alkalin fosfataz ya da çok değerli metal katyonları gibi etkileyiciler sisteme eklendiğinde ebeveyn damlacığın yapısı değişiyor ve bölünme simetrik olmayan bir yola giriyor. Bu tetikleyicilerin, damlacığın katmanları arasındaki etkileşimleri ve ara yüzey davranışını etkileyerek bölünmenin yönünü belirlediği anlaşılıyor. Araştırmacılar, bu sayede yalnızca iki parçaya ayrılmayı değil, ortaya çıkan yavruların morfolojik olarak birbirinden farklı olmasını da sağlayabildi. Bu ayrım, alandaki önceki çalışmaların çoğundan belirgin biçimde ayrılıyor; çünkü daha önce protocel bölünmesi genellikle sıcaklık gradyanları, kimyasal reaksiyonlar ya da ıslanma dinamikleri gibi dışsal etkilerle tetiklenen simetrik fission üzerine kuruluydu.
Yeni çalışmanın dikkat çekici yönlerinden biri, bölünme davranışının biyolojik makinelere benzetilmesine rağmen protein temelli bir düzenek gerektirmemesi. Bu durum, yaşamın en temel süreçlerinden bazılarını yeniden kurmaya çalışan bottom-up sentetik biyoloji açısından özellikle önemli. Proteinler, canlı hücrelerde bölünme, iskelet organizasyonu ve sinyal iletimi gibi işlevlerde merkezi rol oynar. Buna karşın burada gösterilen mekanizma, lipid ve nükleotit temelli bir mimarinin kendi iç fiziksel-kimyasal özellikleri üzerinden yönlendirilmiş bölünme oluşturabileceğini ortaya koyuyor. Başka bir deyişle, araştırma karmaşık biyolojik aygıtlar olmadan da hücresel benzeri davranışların ortaya çıkabileceğini gösteren güçlü bir örnek sunuyor.
Çok katmanlı yapıların sağladığı iç düzen de bu süreçte belirleyici görünüyor. Moleküllerin yoğun biçimde bir arada bulunması, seçici sequestasyon ve kontrollü yüzey etkileşimleri için elverişli bir ortam oluşturuyor. Bu tür moleküler sıkışıklık, biyolojik hücrelerde enzimatik reaksiyonlardan nükleik asit davranışına kadar pek çok süreci etkileyen bir unsur olarak biliniyor. Dolayısıyla lipid-nükleotit damlacıklarının, hem fiziksel hem de kimyasal açıdan hücre benzeri mikroçevreler kurabilmesi, onları yalnızca pasif model sistemler olmaktan çıkarıp işlevsel prototiplere dönüştürüyor.
Çalışma, asimetrik bölünmenin neden bu kadar önemli olduğuna da dolaylı biçimde ışık tutuyor. Eşitsiz bölünme, tek bir yapının farklı kaderlere sahip iki ürün oluşturmasına olanak tanır. Bu, yapay hücrelerde basit çoğalmadan daha ileri bir davranıştır; çünkü bir yavru yapı belirli molekülleri daha çok tutarken diğeri farklı bileşenlere sahip olabilir. Böyle bir özellik, gelecekte yapay sistemlerin görev paylaşımı yapmasına, karmaşık kimyasal süreçlerde uzmanlaşmasına ya da çevresel sinyallere göre farklı yanıtlar üretmesine kapı aralayabilir. Araştırma henüz erken aşamada olsa da, biyolojik çeşitlenmenin fiziksel ilkelerle yeniden kurulabileceğini göstermesi bakımından dikkat çekiyor.
Uzmanlar açısından bir başka önemli nokta da bu bulgunun yapay hücre tasarımında yeni bir kontrol katmanı sunması. Şimdiye kadar protosel araştırmalarında temel soru, bir yapının nasıl oluşturulacağı ve nasıl bölüneceğiydi. Bu çalışma ise bölünmenin nasıl yönlendirilebileceğini ve sonuç ürünlerin nasıl farklılaştırılabileceğini gündeme taşıyor. Bu, sentetik biyolojinin hedefini yalnızca “hücre benzeri parçacıklar” üretmekten, “davranışsal olarak organize olabilen” sistemler kurmaya doğru genişletiyor. Özellikle kimyasal mikroçevrelerin hassas biçimde ayarlanabildiği platformlarda bu tür mekanizmaların daha da geliştirilmesi beklenebilir.
Yine de bulgunun doğal hücrelerin karmaşık bölünme ağlarını tamamen taklit ettiği söylenemez. Araştırma, belirli koşullar altında çalışan bir model sistem sunuyor ve bunun biyolojik organizmaların genetik olarak programlanmış, çok katmanlı kontrol devreleriyle eşdeğer olduğu anlamına gelmiyor. Ancak bilimsel değeri tam da burada yatıyor: Yaşamın temel davranışlarından biri olan asimetrik bölünmenin, proteinlerden arınmış sentetik bir ortamda hangi ilkelerle ortaya çıkabileceği artık daha net görülebiliyor. Bu da gelecekte daha karmaşık yapay hücrelerin tasarımı için sağlam bir zemin oluşturuyor.
Sonuç olarak Meng, Jia, Qiu ve meslektaşlarının Nature’da yayımlanan çalışması, lipid-nükleotit damlacıklarını yalnızca yapı olarak değil, davranış olarak da canlı sisteme yaklaştıran bir dönüm noktasına işaret ediyor. Asimetrik bölünmeyi mümkün kılan bu mekanizma, bottom-up yapay hücre araştırmalarında yeni bir sayfa açabilir. Önümüzdeki dönemde benzer sistemlerin farklı tetikleyicilerle nasıl yönlendirileceği ve bu eşitsiz bölünmenin işlevsel çeşitlilik üretip üretemeyeceği, alanın en önemli soruları arasında yer alacak.

 Denizanasından İlham Alan Manyetik Yumuşak Robot, Biyomedikal Görevlerde Hız Sınırını Aşıyor
Denizanasından İlham Alan Manyetik Yumuşak Robot, Biyomedikal Görevlerde Hız Sınırını Aşıyor
 Çocukluk Çağı Lösemisinde Gen Füzyonlarını Daha Hızlı ve Uygun Maliyetle Saptayan Yeni Yaklaşım
Çocukluk Çağı Lösemisinde Gen Füzyonlarını Daha Hızlı ve Uygun Maliyetle Saptayan Yeni Yaklaşım
 Ameliyatın Öncesinden Sonrasına Uzanan Yeni Model: Perioperatif Tıp Cerrahi Bakımı Yeniden Tanımlıyor
Ameliyatın Öncesinden Sonrasına Uzanan Yeni Model: Perioperatif Tıp Cerrahi Bakımı Yeniden Tanımlıyor






