Now Reading: Pankreas Kanseri ile Obezite ve Diyabet Arasında Ortak İltihap İmzaları Bulundu
-
01
Pankreas Kanseri ile Obezite ve Diyabet Arasında Ortak İltihap İmzaları Bulundu
Pankreas Kanseri ile Obezite ve Diyabet Arasında Ortak İltihap İmzaları Bulundu
University of Birmingham araştırmacıları, pankreas kanseri ile obezite ve tip 2 diyabet arasındaki uzun süredir gözlenen klinik bağa yeni bir genetik açıklama getirdi. Cancer Medicine dergisinde yayımlanan çalışma, pankreatik duktal adenokarsinomun (PDAC) yalnızca tümör biyolojisi açısından değil, aynı zamanda metabolik hastalıklarla paylaştığı iltihap odaklı gen yolları açısından da incelenmesi gerektiğini gösteriyor. Bulgular, bu üç durumun birbirinden bağımsız süreçler olmadığını; en azından bir bölümünde ortak biyolojik mekanizmalar tarafından şekillendirilebileceğini düşündürüyor.
Pankreas kanseri, erken belirtilerinin silik olması ve çoğu zaman ileri evrede fark edilmesi nedeniyle onkolojide en zorlayıcı hastalıklardan biri olarak kabul ediliyor. En yaygın alt tür olan PDAC, mevcut tedavilere karşı direnç geliştirebilmesi ve tanı konulduğunda çoğu hastada hastalığın zaten ilerlemiş olması nedeniyle kötü bir prognozla ilişkilendiriliyor. Klinik gözlemler, obezite ve tip 2 diyabeti olan hastalarda sonuçların daha da olumsuz olabildiğini uzun zamandır ortaya koyuyordu. Ancak bu ilişkinin neden bazı hastalarda daha belirgin olduğu ve hangi moleküler süreçlerin bu tabloyu hazırladığı net değildi.
Çalışmanın başındaki isimlerden Dr. Animesh Acharjee liderliğindeki ekip, bu soruya yanıt aramak için insan ve fare verilerini birlikte değerlendiren bütünleşik bir analiz yaklaşımı kullandı. Araştırmacılar, geniş genetik veri setlerini karşılaştırarak PDAC ile metabolik bozukluklarda ortak biçimde değişen gen ağlarını taradı. Böylece yalnızca tek bir türde gözlenen bulgulara değil, iki farklı biyolojik sistemde de korunmuş sinyallere odaklanıldı. Bu tür çapraz tür karşılaştırmalar, özellikle karmaşık hastalık ilişkilerini çözmede giderek daha önemli bir yöntem olarak öne çıkıyor.
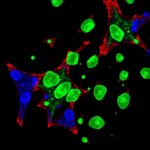
Analizler, inflamasyon ve bağışıklık hücreleriyle ilişkili bazı genlerin hem pankreas tümörlerinde hem de obezite ve tip 2 diyabet bağlamında anlamlı biçimde öne çıktığını gösterdi. ITGAM, PECAM1, CCL5, STAT1, STAT2 ve CD44 gibi genlerin dikkat çekmesi, araştırmanın merkezine tümör mikroçevresi ile metabolik iltihap arasındaki etkileşimi yerleştirdi. Bu genler, bağışıklık hücrelerinin dokuya göçü, hücresel sinyal iletimi ve iltihabi yanıtların düzenlenmesi gibi süreçlerde rol oynuyor. Dolayısıyla bulgular, pankreas kanserinin metabolik hastalıklarda sık görülen kronik düşük düzeyli iltihap zemininden beslenebileceği fikrini güçlendiriyor.
Bilim insanlarına göre önemli noktalardan biri, bu genlerin yalnızca tümör hücrelerinin kendisine değil, aynı zamanda çevresindeki bağışıklık ve stromal yapılara da işaret etmesi. Pankreas tümörleri, yoğun bir tümör mikroçevresiyle çevrili olmaları nedeniyle özellikle karmaşık kabul ediliyor. Bu mikroçevre, kanser hücrelerinin büyümesini destekleyebildiği gibi tedaviye yanıtı da değiştirebiliyor. Obezite ve diyabetle ilişkili metabolik değişikliklerin bu ortamı nasıl yeniden şekillendirdiği ise hâlâ aktif araştırma konusu. Yeni çalışma, bu yeniden şekillenmede iltihabi yolakların merkezi bir rol oynayabileceğini gösteriyor.
PDAC ile metabolik hastalıklar arasında genetik ortaklıklar bulunması, yalnızca hastalıkların nasıl geliştiğini anlamak açısından değil, aynı zamanda risk ve prognoz değerlendirmesi açısından da önem taşıyor. Eğer bu gen imzaları ilerleyen çalışmalarda doğrulanırsa, bazı metabolik profillere sahip hastalarda pankreas kanseri riski ya da hastalığın gidişatı hakkında daha hassas biyobelirteçler geliştirilebilir. Yine de araştırmacılar, mevcut sonucun erken aşama bilimsel bir adım olduğunu ve klinik kullanıma geçmeden önce daha geniş bağımsız kohortlarda doğrulanması gerektiğini vurguluyor.
Bu tür çalışmalar, kanser ve metabolik hastalıkların birbirinden ayrı disiplinler olarak ele alınmasının her zaman yeterli olmadığını hatırlatıyor. Obezite ve tip 2 diyabet, yalnızca pankreas kanseri için genel sağlık durumunu kötüleştiren eşlikçi hastalıklar olarak görülmüyor; aynı zamanda tümör biyolojisini etkileyebilecek moleküler ortamı da değiştirebiliyor. Enflamasyonun bu süreçteki payı, son yıllarda kanser araştırmalarında giderek daha fazla dikkat çeken bir tema haline geldi. Birmingham ekibinin bulguları da tam olarak bu geniş çerçevenin içine oturuyor.
Çalışma, özellikle bağışıklık hücreleri, gen düzenleyici sinyal ağları ve tümör mikroçevresi arasındaki etkileşimin PDAC’de neden bu kadar kritik olduğunu yeniden gündeme taşıdı. Aynı zamanda, metabolik bozuklukların kanser gelişimiyle bağlantısının yalnızca yaşam tarzı düzeyinde değil, doğrudan biyolojik düzeyde de okunması gerektiğini gösteriyor. Araştırmanın bundan sonraki aşamalarında, tanımlanan gen yollarının hastalığın erken evresi, tekrarlama riski ve tedavi yanıtı ile nasıl ilişkili olduğunun daha ayrıntılı incelenmesi bekleniyor.
Sonuç olarak, University of Birmingham’dan gelen bu bulgular pankreas kanseri ile obezite ve tip 2 diyabet arasındaki bağı tek bir iltihap ve gen düzenleme çerçevesinde bir araya getiriyor. Henüz klinik pratiği değiştirecek düzeyde kesinleşmiş olmasa da çalışma, pankreas kanserinin neden bazı metabolik hastalıklarla birlikte daha kötü seyrettiğine dair önemli bir biyolojik ipucu sunuyor. Daha da önemlisi, gelecekte risk sınıflaması ve kişiselleştirilmiş yaklaşım için yeni araştırma kapıları açıyor.