Now Reading: Yenilikçi Kanser Tedavisi için Yeni Protein Yapısı!
-
01
Yenilikçi Kanser Tedavisi için Yeni Protein Yapısı!
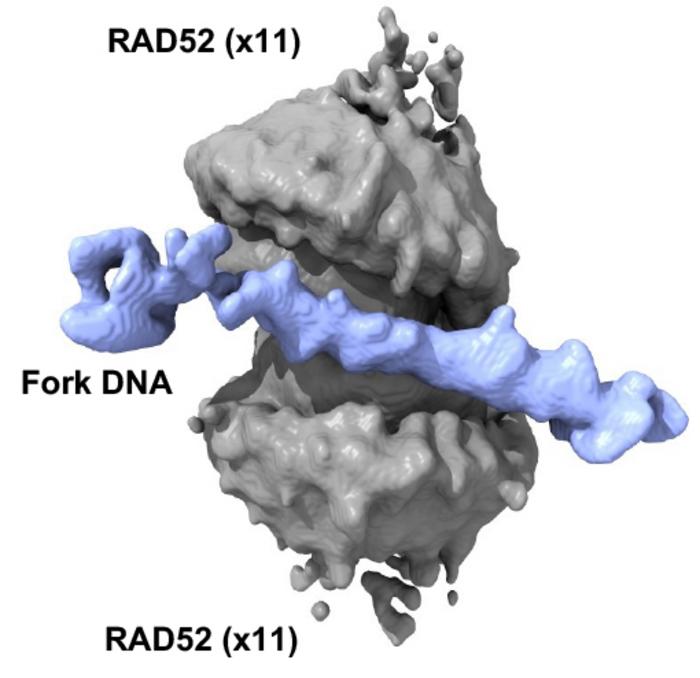
Yenilikçi Kanser Tedavisi için Yeni Protein Yapısı!
Üniversite of Iowa’da gerçekleştirilen çığır açıcı bir araştırma, DNA onarım proteini RAD52’nin DNA ile etkileşimi sırasında ortaya çıkan çarpıcı yeni yapısal konfigürasyonunu gün yüzüne çıkardı. Bu keşfin önemi büyüktür; zira RAD52, özellikle konvansiyonel DNA onarım yollarında eksiklik gösteren kanser hücreleri arasında DNA’yı onarma mekanizmalarında kritik bir rol oynamaktadır. Bu bulgular, RAD52’nin genom bütünlüğünü korumadaki temel rolünü aydınlatmakla kalmayıp, aynı zamanda bu proteine yönelik yenilikçi kanser tedavileri geliştirmek için bir zemin hazırlamaktadır.
Araştırma, 2 Nisan 2025 tarihinde saygın dergi Nature’da yayımlandı ve RAD52’nin DNA ile etkileşim kurduğu moleküler düzeyde nasıl çalıştığına dair karmaşık bir tablo sunmaktadır. Uzman biyokimyacı ve moleküler biyolog Profesör Maria Spies, RAD52’nin DNA ile etkileşim sırasında ortaya çıkan beklenmedik çift halkalı yapısını detaylandırmıştır. Bu benzersiz konfigürasyon, DNA’nın bütünlüğünü korumada çok önemli bir rol oynamakta, özellikle hücresel stresler veya DNA onarımdaki eksiklikler nedeniyle bu süreçlerin bozulduğu durumlarda.
RAD52, özellikle BRCA1 ve BRCA2 mutasyonları gibi genetik zayıflıklar kaynaklı maligniteler için umut verici bir kanser tedavi hedefi olarak dikkat çekmektedir. Geleneksel kanser tedavileri, sağlıklı hücreler ile genetik anormali gösteren hücreler arasındaki farklılıkları göz ardı eden hedefe yönelik yaklaşımlar gerektirmektedir. Araştırma ekibi, RAD52’nin sağlıklı ve kanserli hücrelerin hayatta kalması için gerekli olmadığını, fakat kanser hücrelerinin alternatif DNA onarım mekanizmalarını kullanma eğiliminde olduğunu bulmuştur.
Bu öncü çalışmada kullanılan metodoloji, gelişmiş görüntüleme tekniklerine, özellikle de kriyoelektron mikroskopisine dayanmaktadır. Bu çağdaş yaklaşım, araştırmacıların RAD52-DNA kompleksini eşi benzeri görülmemiş bir ayrıntı ile görselleştirmelerini sağladı. Araştırma, RAD52’nin iki konsantrik halkadan oluşan, her biri on bir RAD52 monomerinden oluşan dikkate değer bir makara benzeri yapı oluşturduğunu ortaya çıkardı. Ayrıca, bu yapı DNA replikasyon çatalının üç kolunu da kapsayarak, yapıyı stabilize etmekte ve bozunmasını engellemektedir. Bu durum, DNA replikasyonunu tamamlama zorunda olan hücreler için kritik bir öneme sahip olmaktadır.
Araştırmanın bir diğer önemli yönü, RAD52 ile DNA arasındaki etkileşimlerin dinamik doğasıdır. Bulunan veriler, bu etkileşimlerin sabit olmadığını, aksine DNA onarım süreçlerini düzenleyen karmaşık moleküler işlemler serisini içerdiğini göstermektedir. Bu dinamikleri anlamak, RAD52’nin işlevini hedef alacak küçük moleküllerin tasarlanmasında kritik öneme sahiptir. Bu sayede sağlıklı dokulardaki normal hücresel işlevleri olumsuz etkilemeden RAD52’nin işlevini inhibe edecek tedavi stratejileri geliştirilebilir.
Önceki çalışmalar, RAD52’nin duraksayan DNA replikasyon çatallarını kurtarma işlevini belirlemiş ve bu özelliğin kanser hücreleri tarafından DNA hasarına rağmen hayatta kalma ve çoğalma amacıyla kullanıldığını göstermiştir. RAD52 tabanlı tedavileri hedef almanın sonuçları kayda değer olabilir; zira bu proteinin engellenmesi, hayatta kalmak için RAD52 işlevine bağımlı kanser hücrelerinde apoptozu tetikleyebilir.
Ayrıca, RAD52 inhibitörlerinin potansiyel terapötik uygulamaları, söz konusu inhibitörlerin etkili bir şekilde kanser hücrelerini yok edebilmesi ve geleneksel kemoterapilerle ilişkili toksik yan etkileri azaltabilmesi nedeniyle güçlenmektedir. Bu özellik, RAD52 inhibitörlerinin BRCA1 ve BRCA2 eksikliklerinden kaynaklanan kanserlerin spesifik zayıflıklarını hedefleyen mevcut tedavi yöntemleri olan PARP inhibitörleri ile birlikte kullanılmasına yönelik bir uyum yaratmaktadır.
Araştırma sonuçlarının klinik uygulamalara geçişini pekiştirmek için elde edilen bulgular son derece değerlidir. Araştırmacıların ortaya koyduğu çift halkalı mimari, ilaç geliştirme için hedeflenebilecek RAD52’nin belirli bölgelerini belirleme konusunda umut vermektedir. Bu doğruluk, mevcut tedavi yöntemlerinin etkisini artırabilir ve sağlıklı hücrelerdeki off-target etkileri en aza indirgeyerek daha kişiselleştirilmiş kanser tedavi seçeneklerine yol açabilir.
Bu araştırmanın dikkat çekici bir yanı, ekibin çok disiplinli işbirliğini yansıtmasıdır. Iowa Üniversitesi bilim insanları ile Roma’daki Istituto Superiore di Sanità uzmanları arasındaki ortaklık, karmaşık biyomedikal soruları çözme konusunda kolektif yaklaşımın önemini gözler önüne sermektedir. Bu işbirliği, bilimsel sorgunun küresel doğasını ve anlamlı yenilikler elde etmek için uzmanlıkların bir araya getirilmesinin gerekliliğini vurgulamaktadır.
Kanser araştırmaları alanı geliştikçe, RAD52 üzerine yapılan sürekli keşiflerin hem kanser biyolojisindeki hem de klinik terapötiklerdeki çok yönlü rolüne dair daha fazla içgörü sağlaması beklenmektedir. Bu çalışmanın sağladığı yapısal revelations, RAD52’yi daha iyi anlamamızın yanı sıra DNA onarımı ile kanser hücresi hayatta kalma arasındaki karmaşık dengeyi de vurgulamaktadır; bu ilişki, kanser biyolojisi ve tedavi stratejilerinin temel taşlarından biridir.
İlerleyen dönemde, araştırma ekibi, Spies laboratuvarından Masayoshi Honda ve Mortezaali Razzaghi’nin önderliğinde RAD52’nin küçük molekül inhibitörlerini daha da geliştirmeyi planlamaktadır. Bu bileşiklerin özgüllüğünü ve etkinliğini artırarak, RAD52’nin bir ilaç hedefi olarak tam potansiyelini kullanmayı ummakta ve bu bağlamda kanser tedavisinde kayda değer bir farklılık yaratmayı hedeflemektedir.
Özetlemek gerekirse, RAD52’nin DNA ile etkileşimi sırasında çift halkalı yapısının keşfi, kanser hücrelerindeki DNA onarım mekanizmalarının anlaşılmasında önemli bir gelişme temsil etmektedir. Bu temel çalışmadan elde edilen bilgiler, RAD52’nin hücresel biyolojideki rolünü derinlemesine anlamanın yanı sıra, bu bilgilerin yenilikçi tedavi stratejilerine dönüştürülmesi konusunda da önemli bir potansiyele sahiptir.
Araştırma Konusu: Kanser hücrelerinde DNA onarımı
Makale Başlığı: RAD52 çift halkası replikasyon çatallarını yeniden şekillendirerek çatal gerilemesini kısıtlar
Haberin Yayınlanma Tarihi: 2 Nisan 2025
Web Referansı: Nature
Makale Referansı: Nature
Resim Credits: Maria Spies, PhD, University of Iowa Health Care
Anahtar Kelimeler: RAD52, DNA onarım, kanser tedavisi, kriyoelektron mikroskobi, moleküler biyoloji, ilaç geliştirme