Now Reading: PRDX1 Susturulması Ferroptozu Tetikleyerek Lenfomayı Durdurur
-
01
PRDX1 Susturulması Ferroptozu Tetikleyerek Lenfomayı Durdurur
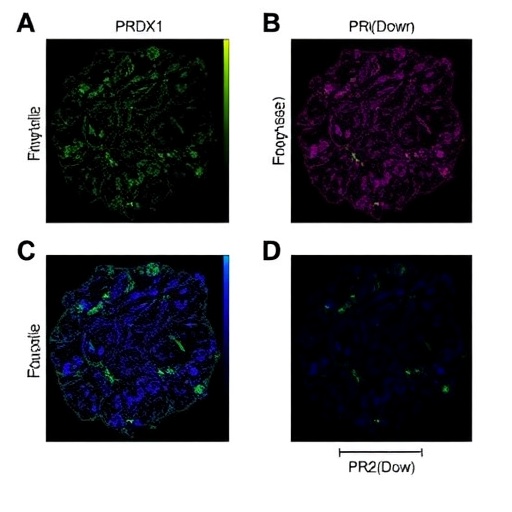
PRDX1 Susturulması Ferroptozu Tetikleyerek Lenfomayı Durdurur
Kanser araştırmalarında çığır açan bir gelişme, yetişkinlerde en yaygın ve agresif lenfoma türlerinden biri olan difüz büyük B hücreli lenfoma (DLBCL) ile mücadelede yeni umutlar sunuyor. Yakın zamanda yayımlanan bir çalışmada, antioksidan enzim Peroksiredoksin 1’in (PRDX1) ferroptozis adı verilen özelleşmiş bir hücre ölümü biçimini nasıl modüle ettiği ortaya kondu. Araştırma, PRDX1’in baskılanmasının hem ferroptozisi artırdığını hem de lenfoma ilerlemesini engellediğini, bu süreçte MAPK/ERK sinyal yolunun bastırıldığını gösteriyor. Bu bulgular, DLBCL tedavisinde yenilikçi stratejiler geliştirmek açısından kritik öneme sahip.
DLBCL, hızlı ilerleyişi ve geleneksel tedavilere karşı direnç göstermesi sebebiyle klinikte önemli bir zorluk oluşturmaktadır. Son yıllarda, demir bağımlı lipid peroksidasyonun yol açtığı programlanmış bir hücre ölümü biçimi olan ferroptozis, kanser tedavisinde yeni bir hedef olarak belirmiştir. Ancak ferroptozisi etkin şekilde tetiklemek klinik uygulamalara taşınırken çeşitli zorluklarla karşılaşılmış, bu da moleküler düzenleyicilerin tanımlanmasının önemini artırmıştır. İşte bu noktada PRDX1, önemli bir regülatör olarak öne çıkmaktadır.
PRDX1, hücre içi redoks dengesinin korunmasında kritik rol oynar ve peroksitleri detoksifiye ederek oksidatif strese karşı hücreleri korur. Ancak kanser biyolojisindeki rolü karmaşıktır; normal hücreleri korurken, stres altında olan kanser hücrelerinin hayatta kalmasını da destekler. Bu çalışma, PRDX1’in DLBCL’de aşırı eksprese edildiğini ve böylece kanser hücrelerini ferroptotik hücre ölümünden koruyarak tümör ilerlemesini desteklediğini ortaya koymuştur.
Araştırmacılar, biyoinformatik analizler ve kantitatif gerçek zamanlı PCR yöntemleri ile PRDX1’in DLBCL dokularında ve hücre hatlarında sağlıklı dokulara kıyasla yüksek düzeyde eksprese edildiğini doğrulamıştır. Artan PRDX1 ifadesi, hücre proliferasyonu ve invazyonunda artışla anlamlı bir şekilde ilişkilendirilmiş, bu da PRDX1’in klinik olarak hedeflenebilecek bir moleküler belirteç olduğunu göstermektedir. Yürütülen hücre içi deneylerde PRDX1 susturulması, lenfoma hücresi viabilitesini olumsuz etkileyerek proliferasyonu engellemiş, göç ve invazyonu sınırlandırmış, aynı zamanda apoptozu teşvik etmiştir.
Çalışmanın önemli bir kısmı, PRDX1 ile ferroptozis arasındaki etkileşimi incelemiştir. Ferroptozis indükleyicisi erastin kullanılarak yapılan deneylerde, PRDX1 silinmiş lenfoma hücrelerinde intracellular demir ve malondialdehit (MDA) seviyelerinin arttığı gözlenmiştir. Bu değişiklikler lipid peroksidasyonunun bir göstergesi olup ferroptozisin etkinleştiğine işaret etmektedir. Aynı hücrelerde glutatyon (GSH) seviyelerinin azalması da ferroptotik sürecin yoğunlaştığını doğrulamıştır. Ek olarak, ferroptozisi engelleyen GPX4 ve SLC7A11 proteinlerinin düzeyinde de azalma kaydedilmiştir.
Moleküler mekanizma açısından, PRDX1’in MAPK/ERK sinyal yolunu düzenlediği ortaya çıkmıştır. PRDX1 susturulduğunda, MEK ve ERK kinazlarının fosforilasyonunda belirgin azalma gözlemlenmiş, bu da MAPK/ERK yolunun aktivitesinde baskılanma anlamına gelmiştir. Bu sinyal yolundaki azalma, DLBCL hücrelerinin malignitesinde düşüş ve ferroptozisin artmasıyla doğrudan ilişkilidir. Böylece PRDX1, MAPK/ERK yolağı üzerinden hücre büyüme ve hayatta kalmasını desteklemektedir.
MAPK/ERK sinyal yolunun rolü, yolağın agonisti olan anisomisin ile yapılan ek deneylerle desteklenmiştir. Anisomisin tedavisi, PRDX1 susturulmasının yol açtığı proliferasyon ve invazyon baskılayıcı etkileri geri çevirmiş, ferroptozisteki artışı da hafifletmiştir. Bu bulgular PRDX1’in kanser üzerindeki etkisinin doğrudan MAPK/ERK sinyal yoluyla aracılık ettiğini ve bu yolun hedef alınmasının terapötik açıdan değerli olabileceğini göstermektedir.
Çalışmanın in vivo modeli olan fare xenograftlarında ise PRDX1 silinmesinin tümör büyümesini belirgin şekilde azalttığı doğrulanmıştır. Bu sonuç, PRDX1’in DLBCL ilerlemesinde vazgeçilmez bir rol oynadığını ve ferroptotik hassasiyeti düzenleyerek kansere karşı mücadelede önemli bir kapı açtığını ortaya koymaktadır. Böylece antioksidan sistem ile demir bağımlı oksidatif hasar arasındaki dengeyi bozarak, PRDX1 baskılanması kanser hücrelerini ferroptozise karşı daha duyarlı hale getirmektedir.
Bu araştırmanın etkileri ve bulguları sadece DLBCL ile sınırlı kalmayabilir. PRDX1, ferroptozis ve MAPK/ERK yolakları arasındaki ilişki, oksidatif stres ve MAPK sinyallemesinin bozulduğu diğer tümör tiplerinde de geçerlilik kazanabilir. Çok katmanlı mekanizmaların hedeflenmesi, monoterapilere karşı gelişen dirençleri aşma ve tedavi etkinliğini artırma açısından avantaj sağlamaktadır.
Klinik açıdan PRDX1, hastalık agresifliği ve tedaviye yanıt için önemli bir biyobelirteç olarak ortaya çıkmaktadır. PRDX1 düzeylerinin ölçülmesi, ferroptozis temelli tedavilere en uygun hastaların tanımlanmasına yardımcı olabilir. Ayrıca PRDX1’in fonksiyonunun baskılanması mevcut kemoterapi ve immünoterapi yaklaşımları ile kombine edilerek daha etkili sonuçlar alınabilir.
Ferroptozis ve onkogenik sinyal yolağı olan MAPK/ERK arasındaki bu kesişme, onkologlar için yeni bir paradigmaya işaret etmektedir. Sadece kanser büyümesini engellemek yerine, düzenlenmiş hücre ölümü yollarını aktive etmek ve aynı zamanda hayatta kalma sinyallerini modüle etmek, dirençli tümörler için ikili bir saldırı stratejisi vaad etmektedir. Özellikle tedavi seçenekleri kısıtlı olan agresif lenfomalar için büyük umutlar taşımaktadır.
Sonuç olarak, bu önemli araştırma PRDX1’in DLBCL hücrelerinin hayatta kalmasını ve ferroptotik duyarlılığını MAPK/ERK yolunu düzenleyerek nasıl yönettiğini ayrıntılarıyla göstermiştir. PRDX1 düzeylerinin azaltılması erastin aracılı ferroptozis indüksiyonunu güçlendirerek tümör hücresi davranışlarını değiştirir ve hastalığın ilerleyişini durdurur. Kanserin redoks biyolojisi alanındaki karmaşıklıkların çözülmesine devam edilirken, bu tür moleküler tespitler kişiye özel etkin tedavilerin geliştirilmesinde yol gösterici olacaktır.
Gelecekte PRDX1 hedefli yaklaşımların ferroptozis indükleyicileri ve MAPK yol modülatörleriyle birleştirilerek kombinasyon terapileri oluşturulması beklenmektedir. Bu bağlamda dozlama, uygulama şekli ve yan etkilerin minimize edilmesi gibi klinik detaylar üzerinde çalışılarak hastaların en iyi şekilde fayda sağlaması amaçlanmaktadır. Bu çalışma; moleküler onkolojinin kanser zırhındaki zayıflıkları tanımlayarak bunları tedavi başarısına dönüştürmedeki gücünü ortaya koymaktadır.
Araştırma Konusu:
Diffuse large B-cell lymphoma (DLBCL) ve peroksiredoksin 1’in (PRDX1) ferroptozis ve MAPK/ERK sinyal yolundaki rolü.
Makale Başlığı:
PRDX1 knockdown promotes erastin-induced ferroptosis and impedes diffuse large B-cell lymphoma development by inhibiting the MAPK/ERK pathway.
Doi Referans:
https://doi.org/10.1186/s12885-025-14173-1
Resim Credits:
Scienmag.com
Anahtar Kelimeler:
Antioksidan enzim, kanser araştırmaları, difüz büyük B hücreli lenfoma, ferroptozis, demir-bağımlı hücre ölümü, lenfoma ilerlemesi inhibisyonu, MAPK/ERK sinyal yolu, moleküler kanser düzenleyicileri, oksidatif stres düzenlemesi, PRDX1 baskılanması, programlanmış hücre ölümü, lenfoma tedavi stratejileri.