Now Reading: Kanser Öncesi Epigenetik İzleri Taıyan Pankreas Hücreleri Genetik Mutasyonlar İçermiyor
-
01
Kanser Öncesi Epigenetik İzleri Taıyan Pankreas Hücreleri Genetik Mutasyonlar İçermiyor
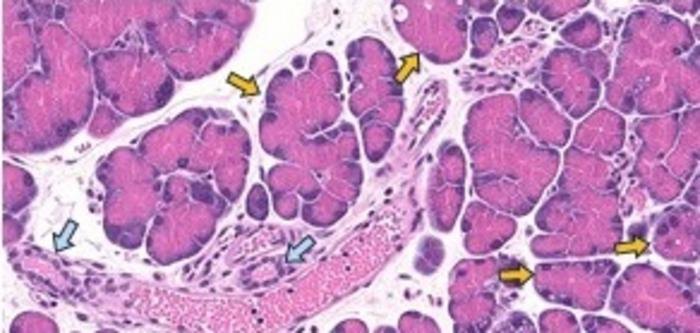
Kanser Öncesi Epigenetik İzleri Taıyan Pankreas Hücreleri Genetik Mutasyonlar İçermiyor
**Johns Hopkins Medicine’den Epigenetik Yüzleşme: Pankreas Kanserinin Kapıları Aralanıyor**
Johns Hopkins Medicine araştırmacıları, pankreatik hücrelerin normal durumdan kanserle ilişkili özelliklerin bulunduğu bir duruma geçişleri sırasında yaşanan epigenetik değişikliklerle ilgili önemli bir keşif yaptılar. Bu bulgular, pankratik kanserin zorlayıcı prognozu ve geç aşamalarda teşhis edilmesi göz önüne alındığında, hastalığın daha iyi anlaşılması için yeni yollar açıyor. Araştırma, inflamasyon ile hücre kimliği dönüşümü arasında önemli bir ilişki ortaya koyuyor. Normal pankreatik hücrelerin, kanserle ilişkili epigenetik işaretlerin bir tür “hafızası” olabileceğini ve genetik mutasyonlar meydana gelmeden önce bile öncül bir kanser potansiyelini barındırdığını vurguluyor.
Pankreasın sindirim enzimlerini üreten akinar hücrelerinin, bir duktal hücrelere dönüşmesi süreci, akinar-ductal metaplazi olarak adlandırılır. Bu dönüşüm, inflamatuar pankreatik ortamdan kaynaklanan bir durumdur ve akinar hücrelerin inflamatuar hasara dayanmasını sağlayan koruyucu bir mekanizma işlevi görür. Bu biyolojik adaptasyon, hücresel biyolojide kritik bir uyum stratejisini vurgularken, normal dokuların patolojik koşullar altında nasıl evrimleşebileceği konusuna ışık tutmaktadır.
Epigenetik değişiklikler, gen ekspresyonunu etkileyen ve DNA dizilimini değiştirmeden gerçekleşen kimyasal değişikliklerdir. Bilgisayar donanımının DNA’yı, yazılımın ise epigenomun işlevini yansıttığı analojisi, bu dinamiği güzel bir şekilde sergiliyor. Gen ekspresyonu, bu epigenetik işaretlerin varlığı veya yokluğu ile dikkatlice düzenlenir. Araştırma, pankreatik hücrelerin normal ve hastalıklı durumlar arasında geçiş yaparken bu değişikliklerin nasıl etki ettiğini özel olarak ele alarak, kanser eğilimli bir çevrede epigenetik manzarayı daha iyi anlamamıza imkan tanıyor.
Andrew Feinberg, M.D. liderliğindeki araştırmacıların, pankreatik hücrelerin bu kritik geçiş aşamasını geçirdiği süre zarfındaki tam epigenetik manzarayı keşfetmek için ileri düzey genomik dizileme teknikleri kullandığı bildirildi. Araştırma sonuçları, pankreatik kanserle ilişkilendirilen genlerde, özellikle PI3K ve R/R/C GTPaz yollarında epigenetik işaretlerin tanımlandığını gösterdi. Özellikle, bu bulgular insan pankreatik öncü lezyonlarında yaygın olarak görülen genetik mutasyonlar olmaksızın ortaya çıktı ve mutagenik olaylar olmadan epigenetik dönüşümün benzersiz bir örneğini oluşturdu.
Bu bulguların etkileri son derece derindir. Pankreatik hücrelerin, kanserle ilişkilendirilen epigenetik değişiklikler ile önceden belirlenmiş bir duruma geçiş yapabileceğini düşündürmekte; bu değişiklikler ise geri döndürülebilir nitelikte olabilir. İltihap ve hücre stresi gibi genetik olmayan faktörlerin kanserle ilişkili geçişleri başlatmadaki etkisinin tanınması, kanser önleme ve müdahale stratejilerini değiştirebilir. Özellikle yaşa bağlı genetik mutasyonların gözlemlenmediği daha genç hastalarda bu durum daha da önem kazanmaktadır.
Araştırmanın bir diğer önemli bulgusu, hücrelerin akinar formuna geri döndüklerinde bile bazı epigenetik işaretlerin tutulmasının, hücresel hafızanın bir türü olduğunu önermesidir. Bu durum, hayatta kalan inflamatuar olayların, gen düzenlemelerinde uzun ömürlü değişiklikler bırakabileceğini ve hücreleri gelecekte neoplastik dönüşümlere hazırlayabileceğini göstermektedir. Bu epigenetik hafıza, pankreatik kanserin erken tanısı için bir biyomarker olarak potansiyel taşıyabilir; bu da klinik belirtiler ortaya çıkmadan önce müdahale fırsatı sunabilir.
Araştırma ayrıca, daha genç demografilerdeki pankreatik kanserin artan görülme oranının sadece genetik predispozisyonlara atfedilemeyeceğini savunuyor. İltihaplı ortamların şekillendirdiği geçiş halleri, gözlemlenen kanser prevalansındaki artışa önemli ölçüde katkıda bulunabilir; bu da onkolojide risk değerlendirmeleri ve önleyici önlemlerin benimsenme biçimini değiştirebilir. Geçiş durumlarına ilişkin daha fazla araştırma, gelecekte hastalığı önleme ve tedavi etme yaklaşımlarını dönüştürebilir.
Araştırmacılar, epigenetik değişikliklerin ve bunların hücresel kimlik üzerindeki etkilerinin derinliğini keşfetmeye devam ederken, bu bulguların yeni terapötik stratejiler geliştirmek için nasıl entegre edilebileceği önemlidir. Normal hücresel süreçlerin epigenetik yolları kullanarak nasıl patolojik bir duruma kayabileceğine dair mekanizmayı anlamak, bu dönüşümleri geri döndürebilir ya da önleyebilir nitelikte müdahaleler tasarlamak için kritik derecede önem taşımaktadır.
Johns Hopkins’teki multidisipliner ekipteki katkılar da bu araştırma için önemli bir bileşeni oluşturmaktadır. İlk yazar Emily Lo ve Patrick Cahan, Ph.D., dahil olmak üzere ekip, epigenetik ve kanser biyolojisi arasındaki bu karmaşık kesişim noktasını aydınlatmak için uyum içinde işbirliği yaptı. Ekiplerinin ortak çabası, pankreatik kanserin evrimiyle ilişkili hücresel ağlar hakkında daha derin bir anlayış geliştirmeye hizmet ediyor ve farklı biyolojik disiplinleri kapsayan hedef araştırma girişimlerinin gerekliliğini vurgulamaktadır.
Sonuç olarak, pankreatik hücre geçişlerinin bu öncü keşfi, kanser biyolojisinin karmaşıklığını vurgulamakla kalmıyor, aynı zamanda pankreatik kanser yönetimi konusunda yenilikçi tanı ve tedavi stratejileri geliştirme umudunu da artırıyor. Araştırmalar ilerledikçe, hücrelerin epigenetik dilini çözme potansiyeli, etkili tedavilerden uzun zamandır kaçan bu sinsice hastalığa karşı mücadelede yeni bir dönem müjdeleyebilir.
Araştırma, genetik mutasyonların kesinlikle kanserin ortaya çıkmasındaki rolünü vurgulasa da, geçiş hallerinde meydana gelen epigenetik değişimlerin özel bir dikkat gerektirdiğini ortaya koymaktadır. Bu değişimlerin ortaya çıkmasını açıklığa kavuşturarak, bilim insanları normal hücreleri kanserli hale getiren dönüşümlerin engellenmesi veya halihazırda değişmiş hücrelerin sağlıklı bir duruma geri döndürülmesi için stratejiler geliştirme konusunda daha iyi bir konumda olabilirler.
Bu araştırma ve bulguları, pankreatik kanserle ilgili halk sağlığı manzarasını önemli ölçüde değiştirebilir. Bilim camiası epigenetik düzenleme katmanlarını ve sonuçlarını daha fazla çözmeye devam ederken, hem kanser mekanizmalarının anlaşılmasını ilerletme hem de daha erken teşhis ve daha kişiye özel tedavi yaklaşımlarını başlatma potansiyeli bulunmaktadır.
Araştırma Konusu: Epigenetik değişikliklerin pankreatik kanser gelişimindeki rolü
Makale Başlığı: Johns Hopkins Research Illuminates Epigenetic Pathways in Pancreatic Cancer
Haberin Yayın Tarihi: 28 Mart 2023
Web References: Genome Medicine
Doi Referans: Belirtilmedi
Resim Credits: Johns Hopkins Medicine
Anahtar Kelimeler: Pankreatik kanser, epigenetik, akinar-ductal metaplazi, inflamatuar yanıt, hücresel dönüşüm, kanser biyolojisi, gen düzenleme, pankreatik öncüler.