Now Reading: Dirençli Lenfoma Hastalarında Çığır Açan CAR-T Tedavisi Başarıları
-
01
Dirençli Lenfoma Hastalarında Çığır Açan CAR-T Tedavisi Başarıları

Dirençli Lenfoma Hastalarında Çığır Açan CAR-T Tedavisi Başarıları
Son yıllarda, dirençli CD30-pozitif lenfomalarla mücadelede önemli bir gelişme yaşandı. Barselona’daki Sant Pau Araştırma Enstitüsü (IR Sant Pau), Sant Pau Hastanesi ve Josep Carreras Lösemi Araştırma Enstitüsü’nün ortak çalışmalarıyla geliştirilen HSP-CAR30 adlı yenilikçi bir kimerik antijen reseptör T-hücresi (CAR-T) terapisi, Hodgkin lenfoma ve bazı T hücreli lenfomalarda bulunan CD30 proteini hedef alacak şekilde özel olarak tasarlandı. Kanser tedavisinde büyük umut vaat eden bu terapi, Peşin Klinik Faz I çalışmasına göre, hafıza T hücrelerinin çoğalmasını tetikleyerek dayanıklı bağışıklık yanıtları oluşturuyor.
Hodgkin lenfoma ve diğer CD30-pozitif lenfomaların yönetimi, özellikle standart tedavilere dirençli ya da relaps gelişmiş vakalarda klinisyenler için ciddi bir zorluk oluşturuyordu. B hücreli maligniteler üzerinde elde edilen başarıya rağmen, CD30-pozitif lenfomalar için CAR-T terapilerinde mühendislik edilen T hücrelerinin kalıcılığının geçici olması ve yüksek nüks oranları tedavinin etkinliğini sınırlandırıyordu. Ayrıca, bu lenfoma tipi üzerine sınırlı klinik deney yapılması, etkili ve uzun süreli tedavi seçeneklerinin geliştirilmesini yavaşlatmıştı. İşte HSP-CAR30, bu engelleri aşmak adına kritik bir dönüm noktası olarak karşımıza çıkıyor.
HSP-CAR30’un yenilikçi yapısı, T hücrelerinin işlevselliği ve ömrünü optimize eden ileri genetik mühendisliği teknikleri içeriyor. Terapide, CD30 antijeninin stabil bir epitopu hedef alınarak, tümör hücrelerinin bağışıklık sisteminden kaçmasına neden olan protein salgılanmasının etkisi azaltılıyor. Buna ek olarak, hücrelerin üretim sürecinde IL-7, IL-15 ve özellikle IL-21 sitokinleri kullanılıyor. Bu sitokinler, henüz tam farklılaşmamış hafıza benzeri T hücrelerinin gelişimini teşvik ederek tedavi etkinliğinin uzun vadeli olmasını sağlıyor.
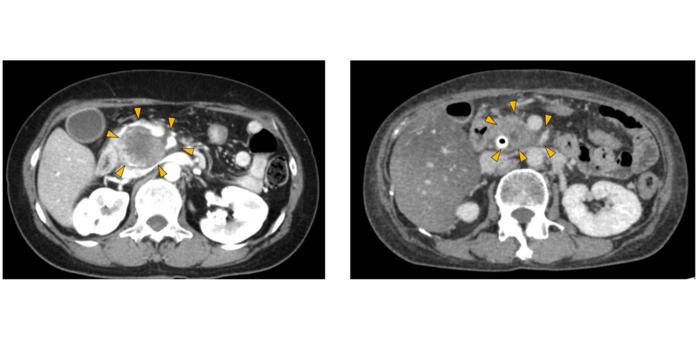
Faz I klinik denemede, relaps veya refrakter klasik Hodgkin lenfoması veya CD30-pozitif T hücreli lenfoma hastası olan 10 kişiye HSP-CAR30 tedavisi uygulandı. Elde edilen sonuçlar son derece çarpıcıydı; %100 genel yanıt oranı tespit edildi. Hastaların yarısında tam remisyon sağlanırken, bu durum görüntüleme ve klinik değerlendirmelerle desteklendi. Tedavi sırasında ciddi doz sınırlayıcı toksisite yaşanmadı; bu da hücre bazlı tedavilerde karşılaşılan yan etki riskinin önemli ölçüde azaltıldığını gösterdi.
Bağışıklık tedavisinde en kritik hedeflerden biri olan yanıtın kalıcılığı üzerine odaklanan takip süreci yaklaşık 3 yıl sürdü. Bu dönemde, tam remisyona ulaşan hastaların %60’ı hastalıksız kalmaya devam etti. Bu durum, HSP-CAR30 pozitif T hücrelerinin dolaşımda devamlılığının sağlanması ile ilişkilendirildi ve hücrelerin kalıcılığı uzun vadeli kanser kontrolünde belirleyici rol oynadı. Nörotoksisite gibi potansiyel ciddi yan etkiler rapor edilmedi; düşük dereceli sitokin salınım sendromu ise küçük hasta grubunda kolayca yönetilebildi.
Terapötik etkinin zirve yaptığı dönemde hastaların hücresel profillerinde merkezi hafıza (TCM) ve kök-benzeri hafıza T hücrelerinin (TSCM-benzeri) yoğunluğunda artış gözlendi. Bu daha az farklılaşmış T hücre alt grupları, proliferasyon kabiliyetleri ve uzun ömürleriyle bilinir. Bu fenotip, önceki CAR-T modellerinden farklı olarak tedavinin uzun vadede etkinliğini ve nüks riskinin azalmasını destekliyor. Böylece, HSP-CAR30, lenfoma nüksü durumunda hızlı ve etkin bir bağışıklık cevabı için dayanıklı bir T hücre rezervi oluşturmayı hedefliyor.
Araştırmayı yöneten uzmanlar, CD30 epitopunun titizlikle seçilmesinin ve T hücrelerinin eks vivo erken evre farklılaşmamış kümelerinin korunmasının terapötik etkinliğin temel taşları olduğunu vurguluyor. Danışman hematolog Dr. Ana Caballero, bu olumlu bulguların daha büyük ölçekli çalışmalarda doğrulanması halinde, dirençli CD30-pozitif lenfomalarda tedavi paradigmasının köklü şekilde değişebileceğini belirtiyor. Böylece, önceden sınırlı tedavi seçeneğine sahip hastalar için yeni umut kapıları aralanıyor.
Başarılı Faz I çalışmanın ardından, çalışma Faz II aşamasına geçerek hasta sayısı 32’ye çıkarıldı ve 10 hasta da veri setine dahil edilmek üzere eklendi. Erken dönem sonuçlarda %55’in üzerinde tam remisyon oranları gözlenmesi, HSP-CAR30’un daha geniş hasta populasyonunda uygulanabilirliğini ve etkinliğini destekliyor. Bu veriler, tedavinin optimize edilerek yasal onay sürecine hız kazandırılması için sağlam bir temel oluşturuyor.
CAR-T terapilerinin çalışma prensibi, hastadan alınan T lenfositlerinin genetik olarak modifiye edilerek tümör yüzey antijenlerini tanımalarının sağlanması ve hastaya yeniden verilerek hedefe yönelik bağışıklık saldırısı gerçekleştirmesidir. HSP-CAR30 yaklaşımı, antijen hedeflemede yapılan iyileştirmeler ve sitokin destekli genişleme sayesinde hem etkinlik hem de hücre kalıcılığı anlamında önceki zorlukların üstesinden geliyor. Böylece T hücresi yorgunluğu ve tümör kaçış mekanizmalarının önüne geçiliyor.
Üretim sürecinde kullanılan IL-21’nin rolü terapinin benzersiz yanlarından biri olarak öne çıkıyor. IL-21, IL-7 ve IL-15 ile birlikte kullanıldığında, daha az farklılaşmış ve uzun ömürlü hafıza T hücresi popülasyonunun oluşmasını destekliyor. Bu hücresel fenotip, hastaların tedavi sonrası uzun süreli bağışıklık gözetimi yapabilmesini sağlayarak hastalığın tekrarlamasını önlemeye yardımcı oluyor. Bu yenilikçi üretim protokolü, önceki CAR-T üretim süreçlerinden önemli bir fark yaratıyor.
Hücre üretimi ve kalite kontrol süreçlerinde yüksek standartlar benimsenmiş durumda. HSP-CAR30 üretim kalite kontrol direktörü Dr. Laura Escribà, hedeflerinin hastalara sadece başlangıçta etkili bir tedavi sağlamak olmadığını, aynı zamanda lenfomanın yeniden ortaya çıkması durumunda hızlı ve etkili müdahale imkanı sunan uzun ömürlü bir hücresel savunma mekanizması geliştirmek olduğunu belirtiyor. Bu kalite güvencesi, terapinin güvenliği ve klinik başarısında kritik önem taşıyor.
HSP-CAR30’un geliştirilmesi ve klinik değerlendirilmesi, Josep Carreras Lösemi Vakfı ile Josep Carreras Lösemi Araştırma Enstitüsü gibi önemli kurumların sağladığı kapsamlı fonlarla desteklendi. “Durmaksızın Hücre Fabrikası” kampanyasıyla, ileri teknoloji hücre üretim tesislerinin finansmanı sağlanarak hasta tedavilerine olanak verildi. Avrupa genelinden kamusal ve özel araştırma fonları ise böyle öncü çalışmalar için hayati önemde olan translasyonel araştırma ortamını oluşturdu.
Avrupa merkezli bu çığır açan çalışma, 2024 Amerikan Hematoloji Derneği (ASH) toplantısında Faz I’in başarılı tamamlanması ve Faz II verilerinin sunulmasıyla önemli bir dönüm noktası elde etti. Çalışma, sadece doğrudan tümör hedeflemenin ötesinde, bağışıklık sisteminin hafıza kapasitesini modüle ederek uzun süreli remisyon sağlama hedefine odaklanan yeni nesil CAR-T geliştirme modelleri için örnek teşkil ediyor. Bu yaklaşım, hastaların yaşam kalitesini ve sağkalımlarını anlamlı biçimde iyileştirecek.
Genetik mühendislik, bağışıklık bilimi ve ileri imalat teknolojilerinin birleşimiyle hayata geçen HSP-CAR30, CD30-pozitif lenfomalarda tedavi perspektifini değiştirecek yenilikçi bir seçenek olarak ön plana çıkıyor. Geniş çaplı çalışmaların benzer sonuçlar vermesi halinde, bu terapi dirençli ya da relaps gelişmiş hastalarda palyatif yaklaşımdan, potansiyel olarak küratif seçeneklere geçişi sağlayacak. Mevcut bulguların yarattığı iyimserlik, kanser immünoterapisinde kalıcı ve kişiye özel tedavi devrimini müjdeliyor.
—
**Araştırma Konusu**: People
**Makale Başlığı**: HSP-CAR30 with a high proportion of less-differentiated T cells promotes durable responses in refractory CD30+ lymphoma
**Haberin Yayın Tarihi**: 17-Apr-2025
**Web References**:
https://doi.org/10.1182/blood.2024026758
http://dx.doi.org/10.1182/blood.2024026758
**Doi Referans**: 10.1182/blood.2024026758
**Resim Credits**: Josep Carreras Leukaemia Research Institute
**Anahtar Kelimeler**:
breakthrough cancer immunotherapy, CAR-T therapy, refractory lymphoma, CD30-positive lymphoma, lymphoma treatment challenges, durable immune responses, engineered T cells, Hodgkin lymphoma innovative therapies, HSP-CAR30 clinical trial, memory T cell expansion, refractory cancer treatment advancements, Sant Pau Research Institute contributions, targeted hematologic cancer therapies