Now Reading: CDI Laboratuvarı, Bağışıklık Hücresi Tükenmesinin Ana Moleküler Sürücüsünü Belirledi
-
01
CDI Laboratuvarı, Bağışıklık Hücresi Tükenmesinin Ana Moleküler Sürücüsünü Belirledi

CDI Laboratuvarı, Bağışıklık Hücresi Tükenmesinin Ana Moleküler Sürücüsünü Belirledi
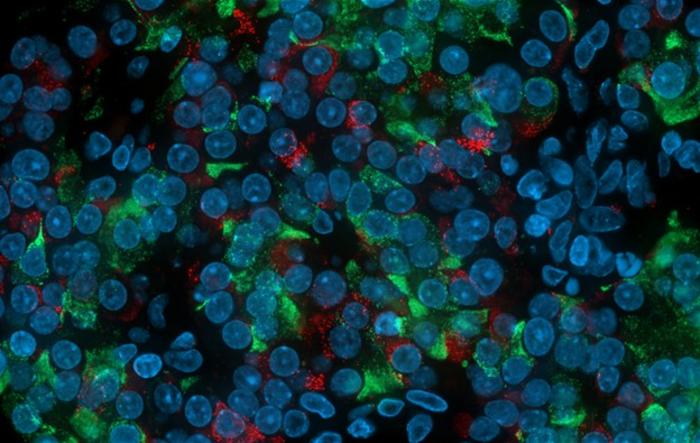
Son yıllarda kanser ve kronik viral enfeksiyonlarla mücadelede bağışıklık sisteminin kritik önemi ortaya çıkarılmıştır. Özellikle CD8+ T hücreleri, yani sitotoksik T lenfositler, enfekte olmuş veya kanserli hücrelerin yok edilmesinde başrolü oynar. Ancak kronik enfeksiyonlar ve bazı kanser türlerinde, bu hücreler uzun süreli antijen maruziyeti nedeniyle fonksiyonlarını yitirip “tükenmişlik” durumuna geçerler. Bu tükenmişlik, sitokin üretiminin azalması, hücresel ölüm yeteneğinin eksilmesi ve çoğalma kapasitelerinin azalması gibi olumsuz sonuçlar doğurur. İşte bu kritik süreç üzerinde moleküler düzeyde yapılan köklü bir araştırma, bu tükenmişlik sürecini durdurmada histon deasetilaz 1 (Hdac1)’in vazgeçilmez rolünü ortaya koydu.
Hackensack Meridian Health bünyesindeki Center for Discovery and Innovation (CDI) araştırma merkezi liderlerinden Dr. Hai-Hui “Howard” Xue ve ekibi tarafından gerçekleştirilen çalışma, Proceedings of the National Academy of Sciences dergisinde yayımlandı. Araştırmacılar, HDAC1 enzimini, CD8+ T hücrelerinin kronik enfeksiyon süresince fonksiyonlarını sürdürmesini ve tükenmişlikten korunmasını sağlayan temel epigenetik düzenleyici olarak tanımladı. Bu bulgu, daha önce kanser tedavisinde kullanılan HDAC inhibitörlerinin bağışıklık hücrelerine olan etkisini sorgulayan yeni bir perspektif kazandırdı.
Histon deasetilaz 1, kromatin yapısında bulunan histonlarının asetil gruplarını uzaklaştırarak gen ekspresyon profilini düzenleyen önemli bir moleküldür. Bu enzim, hücrenin DNA’sının paketlenme biçimini değiştirerek hangi genlerin aktif veya pasif olacağını belirler. Dr. Xue ve ekibi, laboratuvar ortamında oluşturdukları kronik viral enfeksiyon modellerinde, HDAC1’in sürekli aktif kalmasının CD8+ T hücrelerinin fonksiyonel kapasitesinin korunmasında kritik olduğunu gözlemledi. HDAC1 engellendiğinde veya genetik olarak yok edildiğinde, T hücreleri hızla fonksiyonlarını yitirdi ve klasik tükenmişlik profiline geçti.
Ayrıca genom çapında yapılan analizler, HDAC1’in CD8+ T hücrelerinde işleyişini etkileyen gen ağlarını detaylandırdı. Sonuçlar, HDAC1’in, etkili T hücresi farklılaşması ile terminal tükenmişlik epigenetik işaretleri arasında ince bir denge kurduğunu gösterdi. Bu sayede, T hücreleri “ara tükenmişlik” olarak adlandırılan bir aşamada kalabilerek hem çoğalma hem de fonksiyonlarını sürdürebiliyor. Bu moleküler denetleyici mekanizma, kronik bağışıklık cevabında likidite ve esneklik sağlayarak immün yanıtın devamlılığını mümkün kılıyor.
Klinik açıdan bakıldığında, HDAC inhibitörleri genellikle hematolojik ve bazı solid tümörlerin tedavisinde kullanılıyor. Ancak bu çalışmanın gösterdiği üzere, global HDAC inhibisyonu, doğal bağışıklık yanıtında aktif rol oynayan T hücrelerini zayıflatabilir. Bu durum immunoterapilerin etkinliğini azaltabilir veya kanserin bağışıklıktan kaçmasını kolaylaştırabilir. Bu nedenle HDAC inhibitörlerinin kullanımı gözden geçirilmeli, daha seçici yaklaşımlar veya kombinasyon tedavileri geliştirilmelidir.
Araştırma ekibi, önceki çalışmalarda Tle (Transdüsin-like enhancer) aile proteinlerinin, özellikle Tle3’ün CD8+ T hücrelerindeki rolünü inceleyerek epigenetik düzenlemenin bağışıklık homeostazındaki önemini ortaya koymuştu. Yeni bulgu, Hdac1’in benzer şekilde bağışıklık hücrelerinin kaderini belirleyen anahtar düzenleyici olduğunu ve chromatin remodeling yani kromatin yapısının düzenlenmesi yoluyla T hücrelerinin yaşam döngüsü boyunca fonksiyonlarını şekillendirdiğini doğrulamaktadır.
Bu keşifler, koruyucu bağışıklık sağlamak üzere tasarlanan chimerik antijen reseptör (CAR) T hücre terapilerinde yeni hedeflerin belirlenmesini de mümkün kılıyor. CAR-T hücrelerinin tükenmişliğini önlemek için HDAC1 ifadelerinin veya işlevlerinin artırılması, bu hücrelerin kronik bağışıklık zorlukları karşısında dayanıklılığını artırabilir; böylece kanserle mücadelede kalıcı daha etkin cevaplar sağlanabilir. Temel bağışıklık biyolojisi ile klinik uygulamalar arasındaki köprü böylece daha da güçlenmektedir.
Çalışmanın bir diğer önemli noktası ise, kronik enfeksiyon ve kanser ortamlarında CD8+ T hücrelerindeki fonksiyonel çeşitliliğin dengelenmesinde Hdac1 işlevinin belirgin olmasıdır. Epigenetik mekanizmalara bağlı bu denge, hücrelerin hem kendi işlevlerini sürdürmeleri hem de aşırı yorgunluk haline girmemeleri için kritik öneme sahiptir. Bu denge, tedavide yeni ilaç hedeflerinin keşfi ve bağışıklık yanıtının iyileştirilmesi için eşsiz fırsatlar sunmaktadır.
Bununla birlikte, Hdac1’in hangi genlere doğrudan etki ettiği, hangi proteinlerle etkileşimde bulunduğu ve bu mekanizmalardaki zamanlamanın ayrıntıları henüz tam olarak bilinmemektedir. İnsan bağışıklık hücrelerinde ve özellikle tümör mikroçevresinde Hdac1’in rolünün çift yönlü ve karmaşık olabileceği öngörülmektedir. Gelecekte yapılacak çalışmalarla bu sorulara cevap bulunması, tedavi stratejilerinin başarısını artıracaktır.
Özetle, bu son araştırma, kronik bağışıklık stimülasyonu altında CD8+ T hücrelerinin kaderini belirleyen epigenetik bir faktör olarak Hdac1’i ortaya koymuştur. Hdac1 sayesinde, bu hücreler tükenmişlikten uzak kalmakta ve enfeksiyonlar ile tümörlere karşı etkili bağışıklık yanıtlarını sürdürebilmektedir. Elde edilen bulgular, epigenetik enzimlerin modülasyonu ile uzun vadeli bağışıklık koruması ve klinik fayda sağlanmasının önünü açmaktadır.
Bu çalışma, immünoterapide yeni stratejile rin geliştirilmesi için önemli bir yapı taşı oluşturduğundan, özellikle onkoloji alanında hastaların yaşam kalitesini ve tedavi başarısını artıracak yenilikçi yaklaşımlar açısından heyecan uyandırmaktadır. Epigenetik düzenleyicilerin bağışıklık hücre fonksiyonlarındaki bu kritik rolü, gelecekte kanser ve kronik enfeksiyonlarla mücadelede hastalara umut olacak uygulamalara zemin hazırlamaktadır.
—
**Araştırma Konusu**: Animals
**Makale Başlığı**: Hdac1 as an early determinant of intermediate-exhausted CD8+ T cell fate in chronic viral infection
**Haberin Yayın Tarihi**: May 7, 2025
**Web References**: http://dx.doi.org/10.1073/pnas.2502256122
**Doi Referans**: 10.1073/pnas.2502256122
**Resim Credits**: Hackensack Meridian Health
**Anahtar Kelimeler**: Immunology, T cell activation, Immune response, Adaptive immune response, biochemical mechanisms in T cells, cancer immunology research, CD8+ T cells functionality, chronic antigen exposure effects, chronic viral infections, cytokine production decline, epigenetic regulation in immunity, histone deacetylase 1 role, immune cell exhaustion, immunotherapy development, intracellular pathogen defense, T cell vigor maintenance