Now Reading: Toplu RNA Sekanslama, MPN Kliniklerinde Devrim Yaratıyor
-
01
Toplu RNA Sekanslama, MPN Kliniklerinde Devrim Yaratıyor

Toplu RNA Sekanslama, MPN Kliniklerinde Devrim Yaratıyor
Kanser tanı ve kişiselleştirilmiş tıpta genomik teknolojilerin klinik uygulamalara entegrasyonu hızla ilerliyor, ancak bu süreç pek çok zorlukla karşılaşıyor. Philadelphia kromozomu negatif miyeloproliferatif neoplazmlar (MPN’ler) alanında yayınlanan yeni bir çalışma, rutin klinik uygulamalarda kullanılabilecek etkili ve maliyet açısından uygun bir yöntem olarak toplu RNA dizileme (bulk RNA-Seq) yaklaşımını öne çıkarıyor. MPN’ler polistemi vera, esansiyel trombositemi ve primer miyelofibroz gibi kronik kan hastalıklarını içine alıyor. Bu hastalıklar, kompleks mutasyon profilleri ve bağışıklık sistemi düzensizlikleri ile karakterize edilmekte olup, standart klinik uygulamalarda tam olarak değerlendirilememektedir.
MPN’lerde hem sürücü (driver) hem de sürücü olmayan (nondriver) mutasyonlar kök hücrelerde anormal çoğalmaya sebep olurken, aynı zamanda sistemik bir bağışıklık ortamı bozulmasına yol açar. Bu ortamda sitokin üretimi değişikleri ve immün hücre infiltrasyonu komplike bir şekilde etkileşim halindedir. Geleneksel yöntemler, bu karmaşıklığı çözmek için genellikle tek hücre RNA dizileme veya kitle sitometrisi gibi yüksek çözünürlüklü tekniklere başvurmaktadır. Ancak, bu yöntemlerin yüksek maliyeti, teknik karmaşıklığı ve veri işleme zorlukları klinik rutinlere entegre olmasını sınırlandırmaktadır.
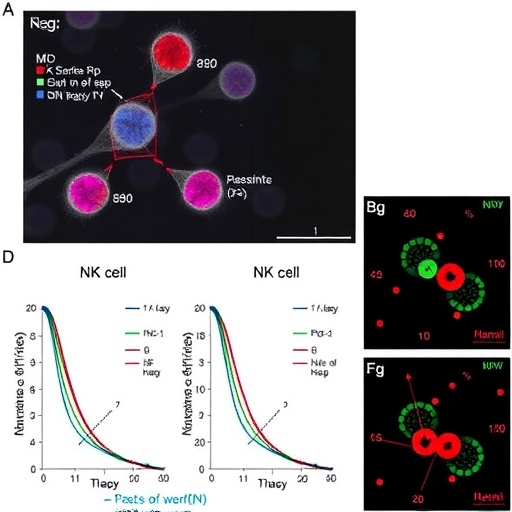
Toplu RNA dizileme bu noktada maliyet etkinliği ve daha basitleştirilmiş analiz özellikleri ile öne çıkıyor. Tek hücre analizlerinden farklı olarak, bulk RNA-Seq örnek içindeki tüm hücrelerin toplam transkriptomunu analiz ederek geniş bir gen ekspresyonu, mutasyon profili ve bağışıklık imzası yelpazesi sunmaktadır. Bahsi geçen çalışmada, tedavi almamış MPN hastalarından alınan periferik kan ve kemik iliği örnekleri bulk RNA-Seq yöntemiyle incelenmiş, böylece hastalığın moleküler temelini ve immün mikroçevresini daha önce görülmemiş bir detayda ortaya koymuştur.
Araştırmacılar deneysel verilerini GSE26049 ve GSE2191 gibi mevcut mikroarray veri kümeleriyle entegre ederek ileri biyoinformatik analitik modeller geliştirmiştir. Bu çapraz-veri yaklaşımı ile gen mutasyonlarına ve bağışıklık ortamı dinamiklerine dair çok boyutlu veriler çözülmüş ve hastalığın seyrini etkileyen kritik genetik değişiklikler ile bağışıklık imzaları tespit edilmiştir. Bu, özellikle yeni tedavilere karşı direnç veya duyarlılık mekanizmalarının anlaşılmasında önemli yol açıcı olmuştur.
Sonuçlar, bulk RNA-Seq’in JAK2, CALR ve MPL gibi sürücü mutasyonları yüksek doğrulukta tespit edebildiğini göstermiştir. Bunların yanı sıra, klonal evrim ve hastalık heterojenitesine katkıda bulunan sürücü olmayan mutasyonlar da tanımlanmıştır. Bu kapsamlı mutasyon analizi, MPN hastalarının prognozunun daha isabetli belirlenmesine ve genetik çeşitliliğe dayalı kişiselleştirilmiş tedavi planlarının geliştirilmesine olanak sağlamaktadır.
Genetik bilgilerle birlikte, çalışma MPN’lerin immün mikroçevresine de derinlemesine bakış sunmaktadır. Bulk RNA-Seq verileri, hastalığın kronik inflamasyon ve immün kaçış mekanizmaları ile karakterize karmaşık immün patolojisini yansıtan farklı bağışıklık hücresi infiltrasyonları ve sitokin profillerini ortaya koymuştur. Bu detaylı bağışıklık profilleme, hem mevcut JAK inhibitörleri gibi tedavilerin etkinliğinin artırılması hem de yeni immünomodülatör hedeflerin belirlenmesi için önemli fırsatlar sunmaktadır.
Çalışmanın en dikkat çekici yanlarından biri, bulk RNA-Seq uygulamasının rutin klinik iş akışlarına entegrasyonunun mümkün olduğunu göstermesidir. Bu, yüksek çözünürlüklü genomik araştırmalarla klinik pratik arasındaki uçurumu kapatarak gelişmiş moleküler tanıya erişimi sadece büyük araştırma merkezlerine değil, yaygın kliniklere de yayma potansiyelini ortaya koymaktadır. Böylece hasta yönetiminde daha hızlı ve bireye özel kararlar alınabilmesine zemin hazırlanmaktadır.
Ek olarak, bulk RNA-Seq ile elde edilen moleküler verilerin klinik parametrelerle birlikte kullanılması hastalık risk gruplarının daha doğru sınıflandırılmasına imkan tanımaktadır. Bu yaklaşım, hastalarda gereksiz toksik etkilerden kaçınarak tedavi yoğunluğunun hastaya göre ayarlanmasını mümkün kılarak, standart tedavilere yanıt vermeyen durumlarda alternatif stratejilerin geliştirilmesine de kapı aralamaktadır.
Bulk RNA dizilemeden ortaya çıkan zengin veri setleri aynı zamanda makine öğrenimi modellerine besin sağlayarak MPN’lerde öngörücü analizlerin yapılmasını kolaylaştırmaktadır. Böylece hastalığın zaman içindeki seyri, tedaviye yanıt veya direnç gelişimi dinamik olarak takip edilerek adaptif onkoloji yaklaşımlarının klinikte uygulanmasına olanak tanınmaktadır.
Çalışmanın bir diğer önemli katkısı, bulk RNA-Seq’in minimal artık hastalık (minimal residual disease-MRD) takibinde kullanılması potansiyelidir. Düşük düzeydeki hastalık yüklerinin konvansiyonel yöntemlerle yakalanması zordur; ancak transkriptom düzeyinde yapılan izlem, tedavi sonrası kalan malign klonların erken saptanarak nüksün önlenmesine yönelik müdahalelerin zamanında yapılmasını sağlayabilir.
Araştırmacılar, bulk RNA-Seq’in hücreler arası heterojeniteyi çözme konusunda sınırlı kaldığını belirtmekle beraber, maliyet etkinliği ve güçlü biyoinformatik destekle klinik tanı ve prognostik süreçlerin ayrılmaz bir parçası haline gelebileceğini vurgulamaktadır. Böylece, detaylı tek hücre analizleri ise daha spesifik ve araştırmaya yönelik durumlar için saklanabilir.
Teknolojik açıdan, çalışma bulk RNA-Seq verilerinden doğru mutasyon tespiti, bağışıklık hücresi çözümlemesi ve yolak analizlerini gerçekleştiren biyoinformatik metodolojiler önermektedir. Veri normalizasyonu, gürültü azaltımı ve varyant alel frekans hesaplamasında geliştirilen algoritmalar ile klinik kullanıma uygun, güvenilir ve uygulanabilir içgörüler sağlanabilmektedir.
Sonuç olarak bu yenilikçi çalışma, bulk RNA-Seq’in rutin MPN kliniklerinde devrim yaratacak bir yaklaşım olduğunu göstermektedir. Genetik ve immün yapıların aynı anda değerlendirilebildiği bu tek seans uygulaması ile tanı, tedavi optimizasyonu ve hastalık takibinde moleküler veriden maksimum fayda sağlanması mümkün hale gelmektedir. Doğrudan klinik pratiğe entegre olunabilmesi, kişiye özel onkoloji bakımında yeni ufuklar açmakta ve hematolojik malignitelerde benzer yöntemlerin yaygınlaşmasına öncülük etmektedir.
Hızla ilerleyen precizyon onkolojisi alanında, bulk RNA-Seq’in pratik kullanımı bilimsel yenilikle klinik uygulanabilirliği birleştiren bir doğru atış olarak değerlendirilmektedir. Klinik çevrelerde daha geniş validasyon ve uygulama platformları geliştikçe, bu teknoloji MPN’lerde hem prognoz hem de tedavi seçimi açısından değerli araçlardan biri olmaya adaydır.
—
Araştırma Konusu: Philadelphia kromozomu negatif miyeloproliferatif neoplazmlar ve rutin klinik uygulamalarda bulk RNA dizileme kullanımı.
Makale Başlığı: Potential application of the bulk RNA sequencing in routine MPN clinics.
Web References: https://doi.org/10.1186/s12885-025-13947-x
Doi Referans: https://doi.org/10.1186/s12885-025-13947-x
Resim Credits: Scienmag.com
Anahtar Kelimeler: bulk RNA sequencing, MPN tanısı, bulk RNA-Seq avantajları, kronik hematolojik maligniteler, genomik teknolojiler, kanser gen ekspresyon profili, hematopoietik kök hücre mutasyonları, MPN’de immün disfonksiyon, gen mutasyon profilleri, kişiselleştirilmiş kanser tedavisi, Philadelphia kromozomu negatif MPN, klinik genomik entegrasyon, kanser tanısında pratik analiz.