Now Reading: Ibrutinib Tedavisi Sonrası NK Hücre Değişikliklerinin Analizi
-
01
Ibrutinib Tedavisi Sonrası NK Hücre Değişikliklerinin Analizi
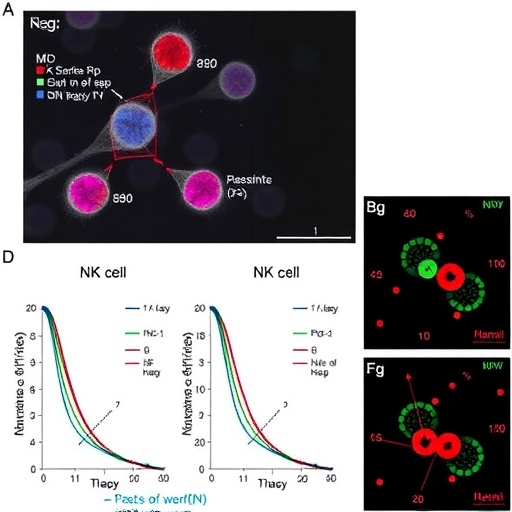
Ibrutinib Tedavisi Sonrası NK Hücre Değişikliklerinin Analizi
Modern onkoloji alanında kronik lenfositik lösemi (KLL) tedavilerinde yeni bir döneme işaret eden önemli bir çalışma, ibrutinib tedavisi sonrası doğal öldürücü (NK) hücre alt gruplarının dinamik değişimlerini tek hücreli transkriptomik yöntemlerle inceleyerek kanser immünolojisi anlayışımızı derinleştiriyor. Araştırmacılar, NK hücrelerinin KLL hastalarında nasıl evrildiğini ve tedaviye yanıt verdiğini moleküler düzeyde ayrıntılı şekilde ortaya koyarak, kişiselleştirilmiş immünoterapi yaklaşımlarının önünü açıyor. Bu gurur verici adım, hedefe yönelik tedavilere yeni bir perspektif kazandırırken, KLL tedavisinde bağışıklık sisteminin daha etkin kullanımının kapılarını aralıyor.
NK hücreleri, bağışıklık sistemimizin doğal savunma hattını oluşturan ve kanserli hücreleri önceden tanımlama gereksinimi olmadan yok etme becerisine sahip kritik efektör hücrelerdir. Ancak, KLL bağlamında, özellikle ibrutinib gibi hedefe yönelik ilaçların kullanımı sonrası NK alt popülasyonlarının davranışlarının ve adaptasyonlarının detayları uzun süredir aydınlatılamamıştı. Bu sorunu ele alan söz konusu çalışma, NK hücrelerinin çeşitliliği, işlevselliği ve moleküler mekanizmalarını hastalık ilerlemesi ve tedavi yanıtı açısından titizlikle ortaya koyuyor.
Araştırmacılar, hastalığın değişik evrelerini temsil eden geniş bir hasta grubundan periferal kandan örnekler topladı. Bu kapsamda monoklonal B hücreli lenfositoz (MBL), yeni tanı almış KLL vakaları (YD-KLL) ve ibrutinib tedavisi sonrası tam ya da kısmi yanıt elde etmiş hastalar yer aldı. Ayrıca, KLL’nin agresif bir dönüşümü olan Richter sendromu hastalarından elde edilen örneklerle, NK hücre davranışlarının tüm klinik spektrumda incelenmesi sağlandı. Bu çeşitlilik, NK hücre alt gruplarının evrimini karşılaştırmalı ve bütüncül şekilde analiz etmeye olanak verdi.
Tek hücre RNA dizileme teknolojisi, her bir NK hücresinin gen ifadesi profillerini ayrı ayrı tarayarak hücre alt tiplerini, bunların genetik imzalarını ve tedavi sonrası yaşanan dinamik değişimleri yüksek çözünürlükte belirledi. Ayrıca “pseüdotemporal analiz” adı verilen hesaplamalı yöntem kullanılarak, NK hücre alt gruplarının gelişimsel ve farklılaşma süreçleri sıralanarak zamansal dönüşüm süreçleri çözümlendi. Böylece ibrutinib sonrası meydana gelen bağışıklık modifikasyonları ayrıntılı şekilde takip edildi.
Çalışmanın sonuçlarına göre üç farklı NK alt grubu tanımlandı: CD56^bright NK hücreleri, bağışıklık düzenlemesinde ve sitokin üretiminde etkin olan; CD56^dim NK hücreleri, güçlü sitotoksik kapasiteye sahip klasik efektörler; ve KLL hastalarına özgü ve yüksek düzeyde sitotoksik özellik taşıyan yeni bir alt grup olan CLL_NK hücreleri. Bu yeni keşfedilen CLL_NK alt grubu, benzersiz bir genetik profil ve fonksiyonel farklılıklar sergileyerek KLL bağlamında özel bir işlevselliğe işaret ediyor.
CLL_NK alt grubunun temel biyolojisini yönlendiren kritik genlerin belirlenmesi için Mendelyan randomizasyon ve genomik colocalization gibi genetik epidemiyoloji yöntemleri kullanıldı. Bu yöntemlerle, genetik veriler tedavi yanıtları ve fenotip ilişkileri bağlamında değerlendirildi ve CLL_NK hücrelerinin fonksiyonunu ve genişlemesini kontrol eden anahtar genler ortaya çıkarıldı. Bu genler, klinik açıdan çekici hedefler olarak immünoterapilerin geliştirilmesinde önem taşıyor.
Araştırmacılar, keşfedilen bu kritik genleri temel alarak, CLL_NK hücre alt grubunun yoğunluğunu ve aktivitesini nicelleştiren özgün bir indeks — CLL_NK İndeksi (CNI) — geliştirdiler. CNI, tedavi yanıtlarını tahmin etme kapasitesiyle, hastaların immünoterapiye verdikleri yanıtların önceden belirlenmesinde kullanılabilecek güçlü bir biyobelirteç olarak işlev görebilir. Böylece kişiye özel tedavi planlamasında önemli bir araç ortaya çıktı.
Bunun yanı sıra, farklı immün infiltrasyon algoritmaları ile NK hücre alt grupları ve tüm bağışıklık mikrouyumu arasındaki karmaşık etkileşim ağları analiz edildi. Bu bütüncül yaklaşım, CLL_NK hücrelerinin immün gözetim mekanizmalarını nasıl şekillendirdiğini ve tümör kaçış süreçlerine nasıl etki ettiğini ortaya koydu. Bu tespitler, KLL’de bağışıklık sisteminin direnç göstermesini engellemek için yeni stratejilerin geliştirilmesine zemin hazırlıyor.
Çalışmanın translasyonel boyutunu güçlendirmek adına ilaç duyarlılık testleri ve moleküler bağlanma simülasyonları gerçekleştirildi. Bu analizler, NK hücre aktivitesini modüle eden veya doğrudan malign B hücrelerini hedef alan semaksanib ve ulixertinib adlı iki ilacı öne çıkardı. Semaksanib’in anjiyogenez inhibitörü, ulixertinib’in ise ERK1/2 kinaz inhibitörü olarak potansiyel sinerjik etkiler sunduğu, böylece bağışıklık kaynaklı kanser hücresi temizliğinin arttırılabileceği belirtildi.
Önemle vurgulanması gereken bir diğer nokta, ibrutinib tedavisi altındaki NK hücre populasyonlarının dinamik plastisitesi. CLL_NK alt grubunun tedavi sırasında genişlemesi ve işlevsel yeniden programlanması, bağışıklığın adaptif yeniden düzenlenmesini yansıtıyor. Bu değişimler, tedavi başarısını artırabileceği gibi, direnç mekanizmalarına da zemin hazırlayabilir. Bu hassas dengenin çözülmesi, tedavi etkinliğini artırmak için yeni imunomodülatör stratejilerin geliştirilmesine ışık tutuyor.
Tek hücre transkriptomik tekniklerin kullanılması sayesinde şimdiye dek gizli kalan hücresel heterojenite ayrıntılı şekilde görülebilmekte. Bu yöntem, toplu RNA dizileme yaklaşımlarınca gözden kaçan mikro düzeyde moleküler özellikleri gün yüzüne çıkararak KLL ve benzeri malignitelerde bağışıklık manzarasının karmaşıklığını güçlendiriyor. Bu teknoloji, kişiselleştirilmiş onkolojide çağ atlatacak bir dönüşümün habercisi niteliğinde.
Sonuç olarak, NK hücre davranışlarının detaylı haritalanması, temel genetik sürücülerin saptanması ve bunların klinik gidişle ilişkilendirilmesi, NK hücre imzalarının rutin prognostik ve terapötik kullanımlarını mümkün kılıyor. Bu gelişme, tedavi seyrinin gerçek zamanlı izlenmesi ve hastaya özgü bağışıklık ortamına uyarlanmış önlemlerin alınmasını sağlayacak yeni bir vizyon sunuyor.
Araştırma, T ve B lenfositlerin ötesinde immün sistem bileşenlerinin de KLL’de kritik rol oynadığını vurgulayarak NK hücrelerinin önemini artırdı. NK hücrelerinin tam potansiyellerinin açığa çıkarılması, hematolojik kanserlerde immunoterapiyi dönüştürebilecek stratejilere ışık tutuyor. Gelecekte CNI’nin daha büyük hasta gruplarında doğrulanması ve CLL_NK modülasyonunun checkpoint inhibitörleri veya CAR-NK terapileri ile kombinasyonlarının araştırılması alanında yeni ufukların kapısı aralanacak.
Özetle, bu öncü çalışma ibrutinib sonrası KLL’de NK hücre alt gruplarını ve genetik profillerini detaylı şekilde ortaya koyarken, ileri düzey tek hücre analizleri, genetik epidemiyoloji ve in-silico ilaç tarama yöntemlerinin entegrasyonunun kanser tedavisinde devrim yaratma potansiyelini vurguluyor. Kişiye özel immün tedavi stratejilerinin geliştirilmesinde kritik bir kilometre taşı olarak kayda geçiyor.
—
Araştırma Konusu:
Kronik lenfositik lösemide ibrutinib tedavisi sonrası doğal öldürücü (NK) hücre alt gruplarının dinamik değişimleri ve spesifik gen imzalarının tek hücre transkriptomiks yöntemiyle incelenmesi.
Makale Başlığı:
Unravelling NK cell subset dynamics and specific gene signatures post-ibrutinib therapy in chronic lymphocytic leukaemia via single-cell transcriptomics
Web References:
https://doi.org/10.1186/s12885-025-14166-0
Doi Referans:
https://doi.org/10.1186/s12885-025-14166-0
Resim Credits:
Scienmag.com
Anahtar Kelimeler:
kronik lenfositik lösemi, doğal öldürücü hücre, NK hücre alt grupları, ibrutinib tedavisi, tek hücre transkriptomik, immünoterapi, CLL_NK alt grubu, genetik imzalar, CLL_NK İndeksi, bağışıklık sistemi adaptasyonu, Richter sendromu, kişiselleştirilmiş kanser tedavisi

























