Now Reading: R-Döngüleri: Genom Kararlılığı ve Hastalıklarda İki Yönlü Rol
-
01
R-Döngüleri: Genom Kararlılığı ve Hastalıklarda İki Yönlü Rol
R-Döngüleri: Genom Kararlılığı ve Hastalıklarda İki Yönlü Rol
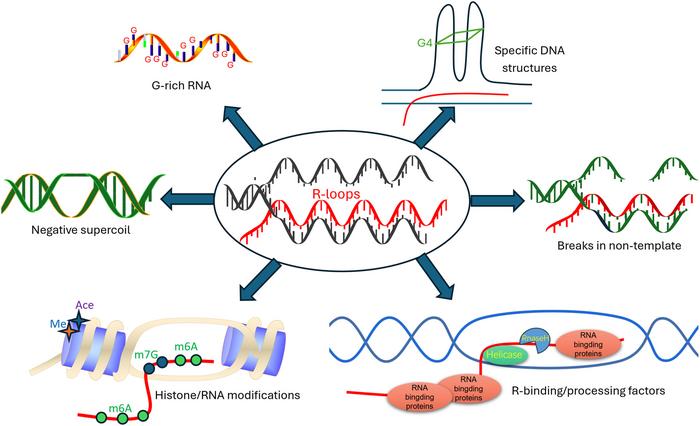
Genomik bütünlüğü koruyan ve bozan çift yönlü yapısıyla dikkat çeken R-loops, moleküler biyolojide giderek daha fazla önem kazanıyor. RNA:DNA hibritinden oluşan ve tek iplikli DNA’nın dışarda kaldığı üçlü yapılar olan R-loops, geçmişte sadece transkripsiyonun yan ürünü olarak görülürken, bugün gen ifadesi, DNA replikasyonu ve tamiri gibi temel süreçlerde kritik düzenleyici elemanlar olarak değerlendiriliyor. Son yıllarda gelişen teknoloji sayesinde bu yapılara ilişkin algımız köklü değişiklikler geçirdi, R-loop’ların hem genom stabilitesini sağlama hem de bozma potansiyeline sahip çok boyutlu roller üstlendiği ortaya çıktı.
Özellikle DNA-RNA immunopresipitasyon sekanslama (DRIP-seq) ve RNA-DNA hibrit immunopresipitasyon ile kromatin immunopresipitasyonu (R-ChIP) gibi ileri teknolojiler R-loop’ların genom çapında yüksek çözünürlükte haritalanmasına imkan tanıyor. Araştırmacılar, bu yapılarının promoter bölgeleri, transkripsiyon sonlandırıcıları ve çift iplik kırık (DSB) yerleşimlerinde yoğunlaştığını belirledi. Bu da R-loop’ların DNA hasar yanıtı mekanizmalarında aktif rol oynadığını kanıtlıyor. Böylece R-loop’lar genomun etkin bekçileri olarak, DNA onarım ve tamir süreçlerinin düzenlenmesinde kritik görevler üstleniyorlar.
R-loop’ların biyolojik doğası paradoksal bir çelişki içeriyor. Normal fizyolojik şartlar altında, kontrollü R-loop oluşumu gen ifadesini düzenleyerek, transkripsiyonun bitişini kolaylaştırarak ve homolog rekombinasyon yoluyla DNA tamirinde rol alarak genom bütünlüğünü koruyor. Bu kontrollü etkileşimler, R-loop’ları gen ifadesini ince ayarlarla kontrol eden dinamik moleküller haline getiriyor. Ancak düzensiz veya aşırı biriktiklerinde, R-loop’lar genotoksik tehditlere dönüşüyor. Replikasyon çatallarının ilerlemesini engelliyor, transkripsiyon ile replikasyon makinelerinin çarpışmasını tetikliyor ve kalıcı DSB’ler yoluyla genomda istikrarsızlığa neden oluyor.
Bu patolojik R-loop birikimi, özellikle BRCA1 ve BRCA2 gibi homolog rekombinasyon tamirinde hayati rol oynayan tümör süpresör genlerde mutasyonların varlığında daha da artıyor. BRCA mutasyonları, R-loop ilişkili genomik istikrarsızlığı tetikleyerek kanser ve nörodejeneratif hastalıklarda sıkça gözlenen bir özellik haline geliyor. Bu nedenle, R-loop disregülasyonunun hastalık etiyolojisi üzerindeki etkisi, onları hem biyobelirteç hem de hedeflenebilir tedavi alanları haline getirdi.
R-loop dinamiklerini ileri düzeye taşıyan faktörler arasında, çeşitli RNA türleri önemli rol oynuyor. Uzun kodlamayan RNA’lar (lncRNAs), dairesel RNA’lar (circRNAs) ve enhançer RNA’lar (eRNAs) R-loop kararlılığını etkileyerek ya belirli R-loop’ları stabilize ediyor ya da çözülmelerini teşvik ediyor. Bu etkileşimler, yerel kromatin yapısını değiştirerek gen ifadesinde ek bir kontrol katmanı oluşturuyor. Böylece RNA-R-loop ilişkileri, genom düzenlemesinde çok yönlü ve kompleks bir mevkiye yükseliyor.
Bir başka önemli katman ise RNA moleküllerinde görülen epitranskriptomik modifikasyonlar. N6-metiladenosin (m6A) ve 5-metilsitozin (m5C) gibi markalar, R-loop oluşumu ve çözülmesinde etkili oluyor. Bu kimyasal değişiklikler RNA’nın DNA’ya bağlanma yeteneğini, stabilitesini ve R-loop metabolizmasında görev alan enzimlerin çekilmesini düzenleyerek DNA tamir süreçlerine doğrudan katkıda bulunuyor. RNA modifikasyonları ile R-loop biyolojisi arasındaki ilişki, gelecekte DNA hasarına karşı stres yanıtlarının anlaşılması açısından önemli kapılar aralıyor.
R-loop’ların etkilediği alanlar sadece nükleer genom stabilitesi ile sınırlı kalmıyor. Son dönemde ortaya çıkan önemli gelişmeler, R-loop’ların sitozolde DNA algılanmasını sağlayan cGAS-STING yolaklarını aktive ederek bağışıklık sisteminin uyarılmasına neden olduğunu gösterdi. Bu durum, DNA hasar denetimi ve enflamatuar reaksiyonların birbirine bağlandığı yeni bir köprü oluşturuyor. Böylece R-loop’lar, hücresel genom bakımı kadar sistemik immün yanıtların düzenlenmesinde de etkili moleküler oyuncular haline geliyor.
Hastalıklar açısından R-loop’lar, terapötik müdahaleler için cazip hedefler sunuyor. Helicase’ler, RNA bağlayıcı proteinler ve RNA modifikasyon enzimlerinin modülasyonu ile R-loop metabolizması üzerinde oynanarak genomik istikrarsızlığın giderilmesi amaçlanıyor. Özellikle homolog rekombinasyon bozukluğu taşıyan kanserlerde, R-loop dinamiklerinin ince ayarlarla düzenlenmesi sağlık için umut vaat ediyor. Küçük moleküller ve gen terapisi yaklaşımları bu alanda geliştirilen önemli stratejiler arasında.
R-loop’lar tek tip yapılardan ziyade, kromatin ortamında çeşitli moleküler faktörlerin etkisiyle dinamik bir denge içinde bulunuyor. Bu kapsamda, R-loop biyolojisinin anlaşılması için genomik, epigenomik ve transkriptomik verilerin entegre edilerek analiz edilmesi gerekiyor. Her genetik ve hücresel bağlamda farklı roller üstlendikleri için bu çok yönlü analizler, potansiyel zayıf noktalar ve hedefler hakkında önemli ipuçları veriyor.
Araştırmalar ilerledikçe R-loop’ların rolü sadece temel moleküler biyolojiyle sınırlı kalmayıp klinik uygulamalara da taşınıyor. Genomik istikrarsızlıkla bağlantılı hastalıklarda R-loop’ların başlangıç ve progresyon sürecine katkılarının ortaya çıkarılması, hassas tanı yöntemleri ve yenilikçi tedavi yolları geliştirilmesini mümkün kılıyor. Buradaki en büyük zorluk, R-loop dengesi korunarak bu yapıların yararlı fonksiyonlarının bozulmaması.
Gelecekte moleküler teknolojiler ve disiplinlerarası yaklaşımların kesişimi ile R-loop, kromatin organizasyonu, epitranskriptom ve bağışıklık sinyallemesinin etkileşimi yüksek mekânsal ve zamansal çözünürlükte aydınlatılacak. Bu veriler, daha etkili ve kişiye özel tedavi stratejilerinin geliştirilmesinde kritik rol üstlenecek. Genom dinamiği ve hastalık mekanizmalarının anlaşılmasını değiştirme potansiyeli taşıyan bu alan, genetik araştırmalarda heyecan verici bir sınırı temsil ediyor.
Sonuç olarak, R-loop’lar hayatın genetik planını korumakta vazgeçilmez yapılar olmalarına karşın, kontrolsüz varlıkları genomik kaosa neden olabiliyor. Bu biyolojik paradoks, R-loop’ları sadece temel bilimde değil, aynı zamanda klinikte de yeni anlayışlar ve çözümler geliştirmek için cazip bir araştırma konusu haline getiriyor. Gelecekte yapılacak çalışmalar, bu üç iplikli yapının hem yaşamı sürdürme hem de hastalıkları tetikleme rollerini daha derinlemesine ortaya koyacak.
—
Araştırma Konusu:
R-loop’ların genomik bütünlükteki rolü, oluşum mekanizmaları, biyolojik fonksiyonları ve insan hastalıklarındaki yeri.
Makale Başlığı:
Update on R-loops in genomic integrity: Formation, functions, and implications for human diseases
Haberin Yayın Tarihi:
2024
Web References:
Genes & Diseases, Volume 12, Issue 4, 2025
Doi Referans:
10.1016/j.gendis.2024.101401
Resim Credits:
Genes & Diseases
Anahtar Kelimeler:
R-loops, genom stabilitesi, DNA tamiri, homolog rekombinasyon, DNA replikasyonu, transkripsiyon regülasyonu, BRCA1, BRCA2, kodlamayan RNA’lar, RNA modifikasyonları, m6A, m5C, cGAS-STING, genomik istikrarsızlık