Now Reading: Hiperaktif Mitokondriler Yaşlanma İlişkili Kan Hastalıklarını Tetikliyor
-
01
Hiperaktif Mitokondriler Yaşlanma İlişkili Kan Hastalıklarını Tetikliyor
Hiperaktif Mitokondriler Yaşlanma İlişkili Kan Hastalıklarını Tetikliyor
Yaşlanmaya bağlı kan hastalıklarının anlaşılmasında köklü bir adım olarak değerlendirilen son araştırmada, The Jackson Laboratory’de görevli bilim insanları, yaşla birlikte artan genetik mutasyonların kan kök hücrelerinin çoğalma kapasitesini nasıl artırdığını detaylı bir biçimde ortaya koydu. Çalışma, hematopoietik kök hücrelerde (kan kök hücreleri) sıkça görülen Dnmt3a mutasyonlarının hücresel metabolizmayı etkileyerek nasıl klonal hakimiyet sağladığını ve bundan doğan hastalıkların önlenmesine dönük yeni tedavi yöntemlerinin kapısını araladı. Bu gelişme, yaşlanmanın kan ve kalp-damar hastalıklarına zemin hazırlamasını moleküler düzeyde anlama konusunda önemli bir ilerleme olarak kabul edilmekte.
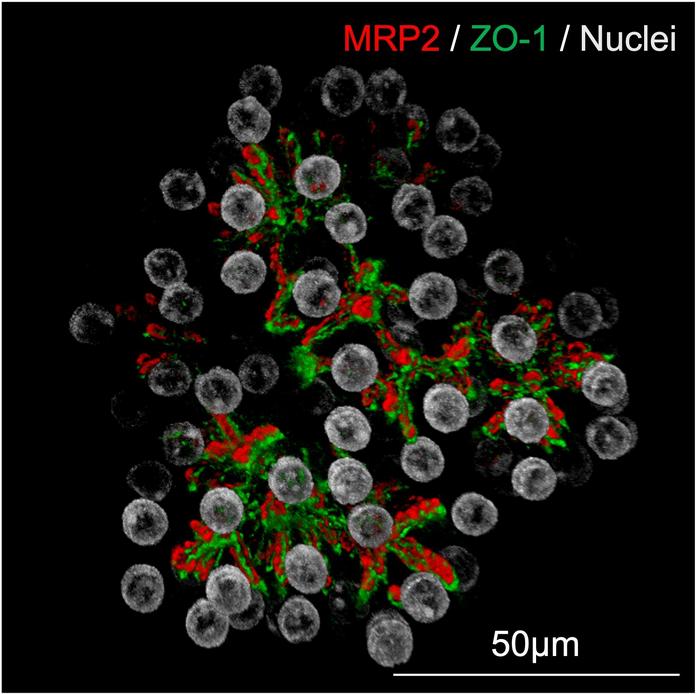
Hematopoietik kök hücreler, kan hücrelerinin sürekli yenilenmesinden sorumlu kritik yapılar olarak, yaş ilerledikçe genetik mutasyon birikimine maruz kalırlar. Bu mutasyonlar arasında, DNA metilasyonunda görev alan ve epigenetik düzenlemede kilit rol oynayan Dnmt3a genindeki değişiklikler hem sayıca yaygın hem de klinik açıdan önemli bulunmuştur. Ancak, Dnmt3a mutasyonlarının normal hücrelerle rekabette üstünlük sağlayarak nasıl çoğalabildiği uzun zamandır tam olarak aydınlatılamamıştı. Jennifer Trowbridge ve ekibinin yürüttüğü bu güncel çalışma, bu süreci metabolik açıdan inceleyerek tamamen yeni bir boyut kazandırdı.
Araştırmada, Dnmt3a mutasyonu taşıyan genetik olarak tasarlanmış fare modellerinde mutant kök hücrelerin mitokondriyal zar potansiyelinin normal hücrelere kıyasla önemli ölçüde yükseldiği tespit edildi. Bu artış, mitokondrilerin enerji üretim kapasitesini (ATP üretimi) ciddi şekilde yükselterek mutant hücreleri adeta “biyolojik olarak aşırı güçlendirilmiş” bir motora dönüştürmektedir. Mitokondriyal bu hiperaktivite, mutant hücrelerin kemik iliği ortamında hızla çoğalmasına ve klonal hematopoezin ortaya çıkmasına yol açmaktadır.
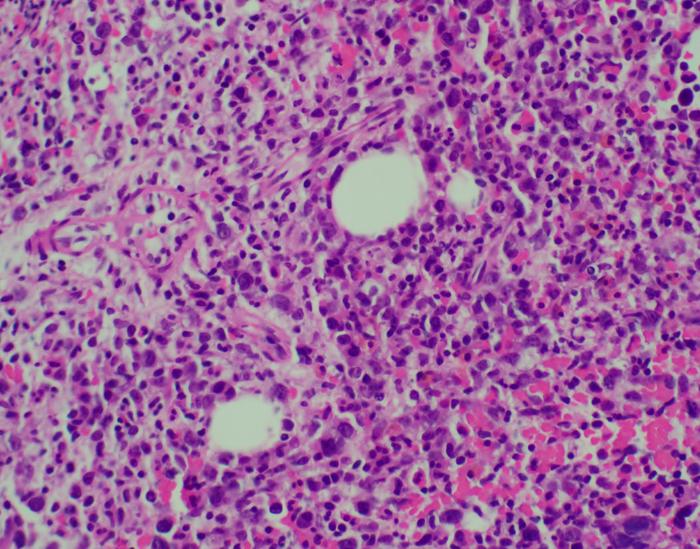
Klonal hematopoez, yaşlı bireylerde bir mutasyonlu progenitör hücreden türeyen kan hücrelerinin çoğunlukta olması durumudur. Klinik olarak önem arz eden bu durum, yaşa bağlı kalp-damar hastalıkları, kan kanserleri ve inflamatuar bozukluklarla güçlü bağlantılıdır. Klonal çoğalmaların sessiz seyri, bu mutant hücrelerin gizli biçimde büyümesine ve hastalığın belirti vermeden ilerlemesine olanak tanımaktadır. Bu nedenle klonal hakimiyetin altında yatan metabolik adaptasyonların çözülmesi, hedefe yönelik ilaç geliştirilmesinde temel bir gerekliliktir.
Araştırmanın heyecan verici yanlarından biri, mitokondriyal aşırı aktivitenin Dnmt3a mutant hücrelerde bir zayıf nokta olarak tanımlanmasıdır. MitoQ ve d-TPP gibi mitokondriye yönelik ajanlarla gerçekleştirilen deneyler, bu bileşiklerin yalnızca mutant kök hücrelerin mitokondriyal işlevini bozarak enerji üretimini engellediğini ortaya koydu. Normal hücrelerin ise mitokondri ATP üretimine bu kadar bağımlı olmaması, bu tedavi seçeneklerinin spesifik ve güvenli bir terapi penceresi sunduğunu işaret etmektedir.
Klinik açıdan dikkat çekici diğer bir bulgu, diabetes ilacı metformin ile paralel alınan sonuçlardır. Metformin, mitokondriyal solunum zinciri aktivitelerini modüle ederek Dnmt3a mutant kök hücrelerin rekabet avantajını azaltmaktadır. Bu ortak etki, mitokondriyi hedef alan tedavi stratejilerinin pratikte uygulanabilirliğini artırmakta ve mevcut ilaçların repurposing (yeniden kullanım) potansiyelini gündeme getirmektedir.
Bu biyogüçlendirme mekanizmasının temelinde, Dnmt3a’nın yalnızca epigenetik düzenleyici bir enzim olmanın ötesinde mitokondriyal metabolizmayı düzenleyen dolaylı bir rolü olduğu ortaya çıkmıştır. Geleneksel anlayışa göre Dnmt3a, DNA metilasyonuyla gen ifadesini kontrol etmekle görevliyken, yeni bulgular onun mitokondri fonksiyonlarını da etkileyerek mutasyona sahip kök hücrelerin metabolik üstünlük kazanmasını sağladığını göstermektedir. Böylece, genetik mutasyonun epigenetik ve metabolik etkileri arasındaki ilişki yeni bir perspektif kazanmıştır.
Bu keşifler, yaşlılarda hematolojik hastalıkların önlenmesine yönelik kişiye özgü tıp uygulamalarına önemli bir ivme kazandırmaktadır. Mutant kök hücrelerin metabolik bir açığı hedefleyen yeni stratejiler, hastalığın belirtiler ortaya çıkmadan önlenmesine olanak tanıyabilir. Bu durum, Dnmt3a mutasyonu taşıyan bireylerde erken tedavi uygulamalarını mümkün kılarak, ileride kan kanseri ve ilişkili kardiyovasküler sorunların önüne geçebilir.
Bununla birlikte, mitokondri hedefli tedavilerin genişletilmesinde dikkat edilmesi gereken bazı faktörler bulunmaktadır. Klonal hematopoezin farklı mutasyonları, çoğalma için farklı metabolik yolları kullanabilir ve mitokondri bağımlılığı her mutasyonda geçerli olmayabilir. Dolayısıyla bu terapötik yaklaşımın genelleştirilebilmesi için farklı mutasyonların metabolik profilleri detaylıca incelenmelidir.
Öte yandan, mitokondriyal fonksiyonların düzenlenmesi çok hassas bir dengeyi gerektirir. Mitokondriler sadece enerji üretmekle kalmaz, aynı zamanda hücre ölümüne (apoptoz), reaktif oksijen türü üretimine ve hücresel sinyallemeye aracılık eder. Tedavilerin hem patojenik klonları ortadan kaldırması hem de sağlıklı kök hücrelerin işlevselliğini koruması bir diğer önemli ölçüttür ve uzun vadeli etkiler incelenmelidir.
İnsan kök hücrelerinde yapılan deneyler, DNMT3A mutasyonu taşıyan hücrelerin mitokondri hedefli inhibitörlere benzer yanıt verdiğini ve proliferatif avantajlarının azaldığını göstermiştir. Bu hayvan modellerinden insana geçiş açısından umut verici bir bulgu olup, klinik uygunluk açısından güçlü bir temel oluşturur. Böylece, mitokondri üzerinde oynanan bu metabolik müdahaleler, insan tedavilerinde yeni bir dönemin sinyalini vermektedir.
Sonuç olarak, genetik, epigenetik ve metabolik araştırmaların entegrasyonu, yaşa bağlı kan hastalıklarının tedavisinde yeni bir paradigma üretmiştir. Mutant kök hücrelerin metabolik destek noktalarını hedef alan stratejiler hastalıkların erken evrede durdurulmasına olanak sağlayarak, molar omurilikteki kan kolonizasyonundan kaynaklanan çeşitli patolojilerin önünü kesebilecektir. Bu yaklaşım, hastaların yaşam kalitesinde ve tedavi sonuçlarında ciddi ilerlemeler vaat etmektedir.
Araştırmanın multidisipliner doğası; moleküler biyoloji, genetik, metabolizma ve farmakolojinin harmanlanmasını gerektirmekte ve bu sinerji, yaşlanma sürecinin hücresel karmaşıklıklarını anlamada kritik önem taşımaktadır. Yaşlanmanın çok yönlü hücresel etkileri açığa çıktıkça, mitokondriyal modülasyon gibi yenilikçi tedavi yöntemleri modern tıbbın yaşlılıkla ilişkili hastalıklarla mücadelesini baştan tanımlayabilir.
Bu çalışmalar ışığında, mitokondri inhibitörleri ve metabolik düzenleyicilerle yapılacak klinik çalışmaların, klonal hematopoezisi tespit edilen yaşlı hastalarda erken dönemde uygulanmasıyla, kanser öncesi ve kardiyovasküler risk azaltıcı bir koruma stratejisi geliştirilebilir. Böylece ileri hastalığa yönelik müdahalelerden önce, hastalık çıkış noktası hedef alınarak, kronik hastalık yükünün azaltılması mümkün hale gelecektir.
—
Araştırma Konusu: Animals
Makale Başlığı: Elevated mitochondrial membrane potential is a therapeutic vulnerability in Dnmt3a-mutant clonal hematopoiesis
Haberin Yayın Tarihi: 16-Apr-2025
Web References:
https://www.nature.com/articles/s41467-025-57238-2
https://www.nature.com/articles/s41586-025-08871-w
Resim Credits: The Jackson Laboratory
Anahtar Kelimeler: Stem cell research, Stem cell therapy, Cancer stem cells, Hematopoietic stem cells, Mutation, Heart disease, Blood cancer, Drug therapy, Disease prevention