Now Reading: Araştırmacılardan Emsalsiz Büyüme Hızına Sahip Mini Karaciğer Modelleri Geliştirildi
-
01
Araştırmacılardan Emsalsiz Büyüme Hızına Sahip Mini Karaciğer Modelleri Geliştirildi
Araştırmacılardan Emsalsiz Büyüme Hızına Sahip Mini Karaciğer Modelleri Geliştirildi
Son yıllarda karaciğer hastalıkları ve rejeneratif tıp alanında yaşanan en önemli gelişmelerden biri olarak, Keio Üniversitesi’nden bilim insanları, insan yetişkin hepatositlerinden oluşan ve metabolik fonksiyonları tam olarak sergileyebilen organoidler geliştirmeyi başardı. Bu üç boyutlu mini karaciğer kültürleri, laboratuvar ortamında insan karaciğerinin karmaşık biyolojik işlevlerini taklit edebilen yeni nesil modeller olarak nitelendiriliyor. Daha önce benzeri görülmemiş metabolik etkinliklere sahip olan bu organoidler, karaciğer hastalıklarının modellenmesinde ve tedavi geliştirme süreçlerinde önemli bir dönüm noktası yaratıyor.
Karaciğerin karmaşıklığı, doku mühendisliği ve hepatoloji alanındaki uzun süredir çözülmeyi bekleyen bir sorun olarak öne çıkıyordu. Diğer organlara kıyasla karaciğer; glukoz regülasyonu, safra asidi salgılanması, protein sentezi gibi çok geniş ve enerjisi yüksek metabolik süreçlerden sorumludur. Buna rağmen laboratuvar ortamında bu fonksiyonları sürdürülebilir şekilde taklit etmek zordur. Tipik olarak, izole hepatositler kültüre alındığında çok kısa sürede fenotiplerini kaybedip safra yollarını döşeyen kolanjiosit benzeri hücrelere dönüşmekte ve hepatositlerin özgün işlevleri bir-iki hafta içinde yok olmaktadır.
Araştırma ekibi, Ryo Igarashi ve Mayumi Oda liderliğinde, doğrudan hastalardan temin edilen dondurulmuş insan yetişkin hepatositlerini kullanarak bu engeli aştı. Çalışmanın temel yeniliği, organoid kültür sistemlerinde daha önce kullanılmamış olan, inflamatuar sinyal yolaklarında görev yapan sitokin onkostatin M’nin uygulanması oldu. Onkostatin M ile tedavi edilen kültürlerde, olağanüstü bir çoğalma evresi gözlemlendi ve organoid sayısı bir milyon kat artış gösterdi. Bu büyüme, daha önce uygulanan yöntemlerle karşılaştırıldığında oldukça çarpıcı ve hepatosit popülasyonlarının kısa sürede yok olduğu eski sistemlerden önemli ölçüde farklılık gösterdi.
Uzun süreli kültürlerde, organoidler üç ay boyunca canlılık ve çoğalma kapasitelerini korudu. Hatta altı aya kadar bu yeteneklerini kaybetmeden devam ettirebildiler. Bu uzun ömürlük yaklaşım, araştırmacıların önce mümkün olmayan uzun süreli fonksiyonel çalışmalar yapmasını ve karaciğer hastalıklarının modellendiği daha gerçekçi deney ortamları yaratmasını sağladı. Ayrıca, ekibin geliştirdiği kimyasal tanımlı hormonal farklılaşma protokolü ile organoidler olgun hepatosit işlevlerini göstermeye başladı. Bu aşamada glukoz, üre, kolesterol, trigliserit ve safra asidi sentezi ve salgılanması gibi temel karaciğer aktiviteleri laboratuvar ortamında yakalanmış oldu.
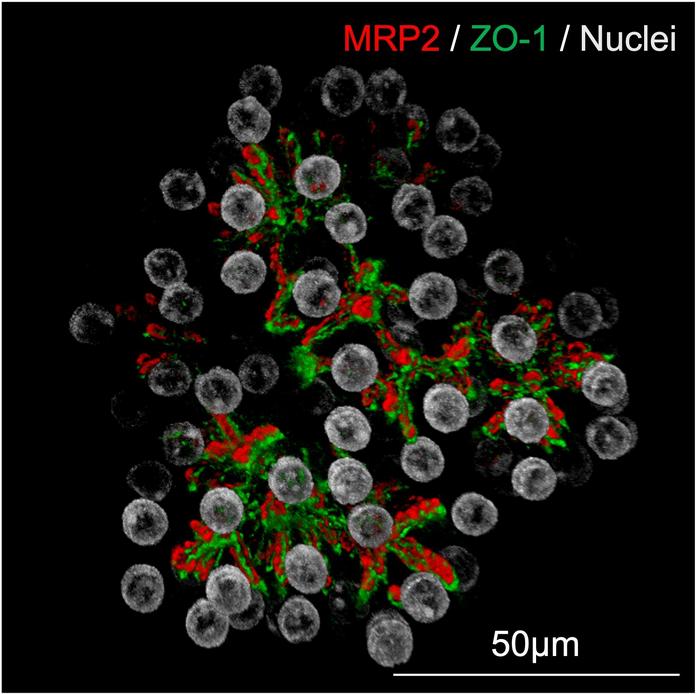
Özellikle dikkat çekici olan, organoidlerin safra kanalıcılarına benzer mikroskobik tübüler yapılar oluşturmasıydı. Bu yapılar, safra asitlerinin taşınmasını mümkün kılarak, karaciğerin özgün mimarisini başarıyla kopyaladı. Böylelikle hepatobiliyer hastalıkların modellenmesi ve safra asidi metabolizmasını hedef alan ilaçların değerlendirilmesi için ideal bir ortam sunuldu. Ayrıca plazmadaki önemli bir protein olan albumin salgısı, mevcut kültür sistemlerine göre daha yüksek seviyelerde belirlendi ve bu, organoidlerin gerçek işlevlerini yansıttığının önemli bir göstergesi oldu.
Onkostatin M’nin hepatosit çoğalmasını tetikleyen kilit bir modülatör olarak tanımlanması teknik bir başarıdan öte, karaciğer biyolojisinin moleküler altyapısına dair yeni bilgiler sundu. Kıdemli araştırmacı Toshiro Sato, bu bulgunun yetişkin karaciğer hücrelerinin rejenerasyon ve farklılaşma potansiyelini “açığa çıkaran” faktörler listesine önemli bir molekül eklediğini belirtti. Önceden sadece sınırlı sayıda molekül organoid büyümesini tetikleyebilmekteyken, onkostatin M sayesinde fonksiyonel karaciğer doku modellerinin çeşitlendirilmesi mümkün hale geldi.
Teknolojinin preklinik modellerde denenmesi de bu yaklaşımın terapötik potansiyelini doğruladı. Bağışıklık sistemi baskılanmış, karaciğer fonksiyonları bozuk farelere insan hepatosit organoidleri nakledildiğinde, organoidler başarılı şekilde yerleşti ve kaybedilen karaciğer hücrelerinin fonksiyonlarını yerine getirdi. Bu gelişme, karaciğer naklinde yaşanan organ bulunabilirliğindeki kritik tıkanıklığı aşmaya yönelik önemli bir adım olarak görülüyor. Donor organların hızla nakledilmesi zorunluluğu ve koruma zorlukları yerine, dondurulmuş hücrelerden türetilen hepatosit organoidlerin talebe göre genişletilip kullanılabilmesi lojistik ve koruma problemlerini esnetiyor.
Ayrıca bu yöntem, geniş ölçekli fonksiyonel karaciğer dokusu üretimini mümkün kılma potansiyeli ile rejeneratif tedavilerde devrim yaratabilir. Sato, organoid çoğalmasının insan karaciğerinin büyüklüğü ve metabolik ihtiyacına yetiştirilmesinin halen aşılması gereken zorluklar arasında olduğunu ancak bunun gerçekleşmesi halinde hastalara yeni yaşam umudu sunacağını vurguladı. Bu sayede ileri evre karaciğer hastalıkları ya da genetik karaciğer bozuklukları tedavisinde çarpıcı gelişmeler yaşanabilir.
Karaciğer hücrelerinden elde edilen organoidlerin ilaç araştırmalarındaki kullanımı da büyük umut vad ediyor. Geleneksel toksisite testleri, kısa ömürlü ve batchler arası tutarsızlık yaşayan taze hepatosit hücreleri kullanılarak yapılıyor. Bu durum, deneylerin güvenilirliğini azaltıp maliyetleri artırıyor. Oysa, organoidler sürekli ve tutarlı bir metabolik aktivite gösteren kaynak sunarak, özellikle hepatotoksik ilaçların geliştirilme sürecini önemli ölçüde kolaylaştırmakta.
Bunların dışında, organoidler hastalık modellemede üstünlük gösterdi. Örneğin, metabolik asit lipid hastalığı (MASLD) tedavisine yönelik ajanlar uygulandığında, organoidlerin iç lipid depoları azaldı. Bu model, önceki çalışmalarda yapay olarak eklenen lipidlerden ziyade, kendi metabolizmasıyla lipid sentezleyen gerçekçi bir ortam sundu. Ayrıca gen düzenleme teknikleriyle, üre döngüsünü bozan nadir genetik hastalık olan ornithine transcarbamylase (OTC) eksikliği gibi durumlar başarılı biçimde taklit edilerek, genetik karaciğer hastalıklarında benzersiz modelleme sağlandı.
İleriye dönük olarak, araştırmacılar organoidlerin karmaşıklığını artırmayı hedefliyor. Karaciğerin tam işlevselliğini anlamak ve tekrar oluşturmak için Kupffer hücreleri (karaciğer makrofajları), karaciğer sinüzoid endotel hücreleri ve hepatic stellat hücreler gibi diğer hücre tiplerinin entegrasyonu büyük önem taşıyor. Ayrıca, klinik uygulamalar için gereken yüksek hücre sayısını karşılamak adına çoğalma kapasitesinin artırılması öncelikli alanlardan biri olmaya devam ediyor.
Sonuç olarak, bu yenilikçi çalışma, insan karaciğerinin karmaşık biyolojisini laboratuvar ortamında yeniden yaratmaya yönelik önemli bir kilometre taşıdır. Yeni sitokin sinyalleme mekanizmaları, gelişmiş farklılaşma protokolleri ve hassas gen düzenleme tekniklerinin entegrasyonu, Keio Üniversitesi araştırmacılarını kişiselleştirilmiş tıp, ilaç keşfi ve rejeneratif tedavilerde yeni ufuklara taşıdı. Karaciğer hastalıklarının küresel sağlık üzerindeki yükü göz önünde bulundurulduğunda, bu organoid modellerinin temel bilim ve translasyonel tıpta vazgeçilmez araçlar haline gelmesi bekleniyor.
Araştırma Konusu: Cells
Makale Başlığı: Generation of human adult hepatocyte organoids with metabolic functions
Haberin Yayın Tarihi: April 16, 2025
Web References: http://dx.doi.org/10.1038/s41586-025-08861-y
Resim Credits: Toshiro Sato from Keio University
Anahtar Kelimeler: hepatocyte organoids, liver regeneration, oncostatin M, organoid proliferation, metabolic functions, liver disease modeling, MASLD, gene editing, urea cycle disorder, transplantation, regenerative medicine